Étiologie et pathogenèse
L’hyperthyroïdie est une sécrétion excessive d’hormones thyroïdiennes, provoquant une accélération de nombreux processus dans l’organisme. C’est l’une des maladies hormonales les plus courantes. Le plus souvent, le développement de l’hyperthyroïdie survient entre 20 et 50 ans. Les femmes sont plus susceptibles de souffrir d'hyperthyroïdie. Parfois, une prédisposition à l'hyperthyroïdie est héréditaire. Le style de vie n'a pas d'importance.
Avec une sécrétion excessive d'hormones thyroïdiennes, de nombreux processus dans le corps reçoivent une stimulation supplémentaire, ce qui conduit à leur accélération. Dans environ 3 cas sur 4, la maladie est causée par la maladie de Basedow, une maladie auto-immune dans laquelle le système immunitaire produit des anticorps qui endommagent le tissu thyroïdien, entraînant une sécrétion accrue d'hormones thyroïdiennes. La maladie de Basedow est héréditaire et on pense qu'elle a une base génétique. Dans de rares cas, l'hyperthyroïdie peut être associée à d'autres maladies auto-immunes, notamment une maladie de peau et un trouble sanguin (anémie pernicieuse).
Symptômes
Les symptômes suivants sont typiques de l'hyperthyroïdie :
Perte de poids malgré un appétit accru et une consommation alimentaire accrue ;
Battement de coeur rapide, souvent accompagné d'arythmie ;
Tremblement (tremblement) des mains ;
Peau trop chaude et humide, en raison d’une transpiration accrue ;
Mauvaise tolérance à la chaleur ;
Anxiété et insomnie ;
Augmentation de l'activité intestinale ;
Formation de tumeur dans le cou causée par une hypertrophie de la glande thyroïde ;
Faiblesse musculaire;
Troubles menstruels.
Les patients souffrant d'hyperthyroïdie causée par la maladie de Basedow peuvent également avoir les yeux exorbités.
Diagnostic et traitement
Si vous soupçonnez le développement d'une hyperthyroïdie, vous devez effectuer un test sanguin pour déterminer l'augmentation du taux d'hormones thyroïdiennes dans le sang et la présence d'anticorps qui endommagent le tissu thyroïdien. Si une tumeur est ressentie dans la région de la glande thyroïde, un test aux radionucléides doit être effectué pour vérifier la présence de nodules dans la glande.
Il existe trois traitements principaux pour abaisser les niveaux d’hormones thyroïdiennes. La plus courante consiste à utiliser . Cette méthode est utilisée pour traiter l'hyperthyroïdie causée par la maladie de Basedow. La méthode vise à supprimer la sécrétion d'hormones thyroïdiennes. Le traitement à l'iode radioactif est la méthode la plus efficace pour la formation de nodules dans la glande thyroïde. Le cours consiste en des doses d'iode radioactif consommées par le patient sous forme de solution. L'iode s'accumule dans la glande thyroïde et la détruit.
De nombreux patients se rétablissent complètement grâce au traitement. Cependant, une rechute de l'hyperthyroïdie est possible, notamment chez les patients atteints de la maladie de Basedow. Lors d’une intervention chirurgicale ou d’un traitement à l’iode radioactif, la partie restante de la glande thyroïde peut ne pas être en mesure de produire suffisamment d’hormones. Il est donc très important de vérifier régulièrement vos niveaux d’hormones après le traitement.
RCHR (Centre républicain pour le développement de la santé du ministère de la Santé de la République du Kazakhstan)
Version : Protocoles cliniques du ministère de la Santé de la République du Kazakhstan - 2017
Thyrotoxicose [hyperthyroïdie] (E05), Thyrotoxicose, sans précision (E05.9), Thyroïdite chronique avec thyrotoxicose transitoire (E06.2)
Endocrinologie
informations générales
Brève description
Approuvé
Commission mixte sur la qualité des soins de santé
Ministère de la Santé de la République du Kazakhstan
du 18 août 2017
Protocole n°26
Thyrotoxicose(hyperthyroïdie) est un syndrome clinique provoqué par un excès d'hormones thyroïdiennes (TG) dans le sang et par leur effet toxique sur divers organes et tissus.
"Thyrotoxicose avec goitre diffus (goitre toxique diffus, maladie Tombes, Bazedov)" est une maladie auto-immune qui se développe à la suite de la production d'anticorps contre la rTSH, se manifestant cliniquement par des lésions de la glande thyroïde avec le développement d'un syndrome de thyréotoxicose en association avec une pathologie extrathyroïdienne (ophtalmopathie endocrinienne (EOP), myxœdème prétibial, acropathie ). La combinaison simultanée de tous les composants du processus auto-immun systémique est relativement rare et n'est pas nécessaire pour le diagnostic (niveau A). Dans la plupart des cas, la plus grande signification clinique dans la thyréotoxicose avec goitre diffus est la lésion thyroïdienne.
Thyrotoxicose chez les patients atteints nœud/multi-nœud le goitre est dû au développement de l'autonomie fonctionnelle du ganglion thyroïdien. L'autonomie peut être définie comme le fonctionnement des cellules folliculaires thyroïdiennes en l'absence du principal stimulateur physiologique - la TSH hypophysaire. Dotées d'une autonomie fonctionnelle, les cellules thyroïdiennes échappent au contrôle de l'hypophyse et synthétisent des TG en quantité excessive. Si la production de TG par des formations autonomes dépasse le besoin physiologique, le patient développe une thyréotoxicose. Un tel événement peut survenir à la suite de l'évolution naturelle du goitre nodulaire ou après que des quantités supplémentaires d'iode ont pénétré dans l'organisme avec des suppléments d'iode ou dans le cadre d'agents pharmacologiques contenant de l'iode. Le processus de développement de l'autonomie fonctionnelle dure des années et conduit à des manifestations cliniques d'autonomie fonctionnelle, principalement chez les personnes plus âgées (après 45 ans) (niveau B).
PARTIE INTRODUCTIVE
Code(s) CIM-10 :
| CIM-10 | |
| Code | Nom |
| E05 | Thyrotoxicose [hyperthyroïdie] |
| E 05.0 | Thyrotoxicose avec goitre diffus |
| E 05.1 | Thyrotoxicose avec goitre uninodulaire toxique |
| E 05.2 | Thyrotoxicose avec goitre multinodulaire toxique |
| E 05.3 | Thyrotoxicose avec ectopie du tissu thyroïdien |
| E 05.4 | Thyrétoxicose artificielle |
| E 05.5 | Crise thyroïdienne ou coma |
| E 05.8 | Autres formes de thyréotoxicose |
| E 05.9 | Thyrotoxicose, sans précision |
| E 06.2 | Thyroïdite chronique avec thyréotoxicose transitoire |
Date d’élaboration/révision du protocole : 2013 (révisé en 2017).
Abréviations utilisées dans le protocole :
| ACI | - | thyroïdite auto-immune |
| BG | - | Maladie de Graves |
| TG | - | les hormones thyroïdiennes |
| TSH | - | hormone stimulant la thyroïde |
| MUTZ | - | goitre toxique multinodulaire |
| TA | - | adénome thyréotoxique |
| T3 | - | triiodothyronine |
| T4 | - | thyroxine |
| glande thyroïde | - | thyroïde |
| LANGUETTE | - | biopsie par aspiration à angle fin de la glande thyroïde |
| PTG | - | parathgorgomon |
| hCG | - | gonadotrophine chorionique humaine |
| AT à TPO | - | anticorps contre la thyroperoxydase |
| AT à TG | - | anticorps contre la thyroglobuline |
| AT en rTSH | anticorps contre le récepteur TSH | |
| je 131 | - | iode radioactif |
| intensificateur d'image | - | ophtalmopathie endocrinienne |
Utilisateurs du protocole : médecins urgentistes, médecins généralistes, thérapeutes, endocrinologues.
Échelle du niveau de preuve:
| UN | Une méta-analyse de haute qualité, une revue systématique d'ECR ou d'ECR de grande envergure avec une très faible probabilité (++) de biais, dont les résultats peuvent être généralisés à une population appropriée. |
| DANS | Revue systématique de haute qualité (++) d'études de cohorte ou cas-témoins ou d'études de cohorte ou cas-témoins de haute qualité (++) avec un risque de biais très faible ou d'ECR avec un risque de biais faible (+), les résultats de qui peut être généralisé à une population appropriée. |
| AVEC | Étude de cohorte ou cas-témoins ou essai contrôlé sans randomisation avec un faible risque de biais (+), dont les résultats peuvent être généralisés à la population concernée ou ECR avec un risque de biais très faible ou faible (++ ou +), dont les résultats ne peuvent être directement diffusés à la population concernée. |
| D | Série de cas ou étude non contrôlée ou avis d’expert. |
| MPE | Les meilleures pratiques cliniques recommandées sont basées sur l'expérience clinique des membres du groupe de travail CP. |
Classification
Àclassification:
1) Thyrotoxicose causée par une production accrue d'hormones thyroïdiennes :
Maladie de Basedow (GD) ;
· adénome toxique (AT) ;
hyperthyroïdie induite par l'iode ;
· phase hyperthyroïdienne de la thyroïdite auto-immune (AIT) ;
· TSH - hyperthyroïdie conditionnée.
− adénome hypophysaire producteur de TSH ;
− syndrome de sécrétion insuffisante de TSH (résistance des thyréotrophes aux hormones thyroïdiennes).
· hyperthyroïdie trophoblastique.
2) Hyperthyroïdie causée par la production d’hormones thyroïdiennes en dehors de la glande thyroïde :
· métastases du cancer de la thyroïde produisant des hormones thyroïdiennes ;
Chorinonépithéliome.
3) Thyrotoxicose non associée à une hyperproduction d'hormones thyroïdiennes:
· thyréotoxicose d'origine médicamenteuse (surdose d'hormones thyroïdiennes) ;
· la thyréotoxicose, en tant que stade de la thyroïdite subaiguë de Quervain, de la thyroïdite post-partum.
Tableau 2. Classification des tailles de goitre
:
Tableau 3. Classification et pathogenèse de la thyréotoxicose :
| Forme de thyréotoxicose | Pathogenèse de la thyréotoxicose |
| Maladie de Graves | Anticorps stimulant la thyroïde |
| Adénome thyroïdien thyréotoxique | Sécrétion autonome d'hormones thyroïdiennes |
| Adénome hypophysaire sécrétant de la TSH | Sécrétion autonome de TSH |
| Thyrotoxicose induite par l'iode | Excès d'iode |
| AIT (hasitoxicose) | Anticorps stimulant la thyroïde |
| Destruction des follicules et entrée passive des hormones thyroïdiennes dans le sang (calloïdorragie) | |
| Thyrotoxicose médicamenteuse | Surdosage de médicaments pour la thyroïde |
| Tératome ovarien sécrétant T4 et T3 | Sécrétion autonome d'hormones thyroïdiennes par les cellules tumorales |
| Tumeurs qui sécrètent de l'hCG | Action de type TSH de l'hCG |
| Mutations du récepteur TSH | |
| Syndrome de McCune-Albright-Britsev | Sécrétion autonome d'hormones thyroïdiennes par les thyrocytes |
| Syndrome de résistance aux hormones thyroïdiennes | Effet stimulant de la TSH sur les thyrocytes en raison du manque de rétroaction |
Diagnostique
MÉTHODES, APPROCHES ET PROCÉDURES DE DIAGNOSTIC
Critères diagnostiques
Plaintes et anamnèse :
Plaintes
sur le:
· nervosité ;
· transpiration ;
· battement de coeur;
· fatigue accrue;
· augmentation de l'appétit et, malgré cela, perte de poids ;
· faiblesse générale ;
· labilité émotionnelle;
essoufflement;
· troubles du sommeil, parfois insomnie ;
· mauvaise tolérance aux températures ambiantes élevées ;
· diarrhée;
· inconfort oculaire - sensations désagréables au niveau des globes oculaires, tremblements des paupières ;
· troubles du cycle menstruel.
DANS antécédents médicaux:
· présence de proches souffrant de maladies thyroïdiennes ;
· maladies respiratoires aiguës fréquentes ;
· processus infectieux locaux (amygdalite chronique).
Examen physique :
· augmentation de la taille de la glande thyroïde ;
· troubles de l'activité cardiaque (tachycardie, bruits cardiaques forts, parfois souffle systolique au sommet, augmentation de la pression artérielle systolique et diminution de la pression artérielle diastolique, crises de fibrillation auriculaire) ;
· troubles du système nerveux central et sympathique (tremblements des doigts, de la langue, de tout le corps, transpiration, irritabilité, sentiments d'anxiété et de peur, hyperréflexie) ;
· troubles métaboliques (intolérance à la chaleur, perte de poids, augmentation de l'appétit, soif, croissance accélérée) ;
· troubles du tractus gastro-intestinal (selles molles, douleurs abdominales, augmentation du péristaltisme) ;
symptômes oculaires (large ouverture des fentes palpébrales, exophtalmie, regard effrayé ou méfiant, vision floue, vision double, décalage de la paupière supérieure en regardant vers le bas et de la paupière inférieure en regardant vers le haut).
Environ 40 à 50 % des patients atteints de MH développent intensificateur d'image, qui se caractérise par des lésions des tissus mous de l'orbite : tissu rétrobulbaire, muscles extraoculaires ; impliquant le nerf optique et l’appareil auxiliaire de l’œil (paupières, cornée, conjonctive, glande lacrymale). Les patients développent des douleurs rétrobulbaires spontanées, des douleurs lors des mouvements oculaires, un érythème des paupières, un œdème ou un gonflement des paupières, une hyperémie conjonctivale, une chémosis, une exophtalmie et une mobilité limitée des muscles extraoculaires. Les complications les plus graves de l'EOP sont : la neuropathie optique, la kératopathie avec formation d'une cataracte, la perforation cornéenne, l'ophtalmoplégie, la diplopie, du système musculaire (faiblesse musculaire, atrophie, myasthénie grave, paralysie périodique)).
Recherche en laboratoire :
Tableau 4. Paramètres de laboratoire pour la thyréotoxicose :
| Test* | Les indications |
| TSH | Réduit à moins de 0,1 mUI/l |
| T4 gratuit | Promu |
| T3 gratuit | Promu |
| AT à TPO, AT à TG | Promu |
| AT au récepteur TSH | Promu |
| RSE | Augmentation dans la thyroïdite subaiguë de Quervain |
| Gonadotrophine chorionique humaine | Augmentation du choriocarcinome |
Certains patients présentent une diminution des taux de TSH sans augmentation simultanée de la concentration d'hormones thyroïdiennes dans le sang (niveau A). Cette affection est considérée comme une thyréotoxicose subclinique, sauf si elle est due à d'autres raisons (prise de médicaments, maladies graves non thyroïdiennes). Un taux de TSH normal ou élevé dans le contexte de taux élevés de fT4 peut indiquer un adénome hypophysaire producteur de TSH ou une résistance sélective de l'hypophyse aux hormones thyroïdiennes. Des anticorps anti-TSH sont détectés chez 99 à 100 % des patients atteints de thyréotoxicose auto-immune (niveau B). Pendant le traitement ou la rémission spontanée de la maladie, les anticorps peuvent diminuer, disparaître (niveau A) ou modifier leur activité fonctionnelle, acquérant des propriétés bloquantes (niveau D).
Des anticorps anti-TG et TPO sont détectés chez 40 à 60 % des patients atteints de goitre toxique auto-immun (niveau B). Lors de processus inflammatoires et destructeurs de la glande thyroïde de nature non auto-immune, des anticorps peuvent être présents, mais en faibles niveaux (niveau C).
La détermination systématique du taux d'anticorps anti-TPO et TG pour le diagnostic de DTG n'est pas recommandée (niveau B). La détermination des anticorps anti-PTO et TG est effectuée uniquement pour le diagnostic différentiel de la thyréotoxicose auto-immune et non auto-immune.
Etudes instrumentales :
Tableau 5. Études instrumentales pour la thyréotoxicose :
| Méthode de recherche | Note | DU |
| Ultrason |
Le volume et l'échostructure de la glande thyroïde sont déterminés. En HD : augmentation diffuse du volume de la glande thyroïde, l'échogénicité de la glande thyroïde est uniformément réduite, l'échostructure est homogène, l'apport sanguin est augmenté. Avec AIT : hétérogénéité d'échogénicité. Avec MUTZ : formations dans la glande thyroïde. Dans le cancer de la thyroïde : formations hypoéchogènes avec contours inégaux du ganglion, croissance du ganglion au-delà de la capsule et calcification. |
DANS |
|
Scintigraphie de la glande thyroïde. L'isotope utilisé est le technétium 99mTc, I 123, plus rarement I 131. |
En HD, il y a une augmentation et une distribution uniforme de l'isotope. Avec l'autonomie fonctionnelle, l'isotope s'accumule dans un nœud fonctionnant activement, tandis que le tissu thyroïdien environnant est dans un état de suppression. En cas de thyroïdite destructrice (subaiguë, post-partum), la captation du radiopharmaceutique est réduite. TA et MUTZ sont caractérisés par des « ganglions chauds », tandis que le cancer est caractérisé par des « ganglions froids ». |
UN |
| La scintigraphie thyroïdienne est indiquée pour MUTZ, si le taux de TSH est inférieur à la normale, ou à des fins de diagnostic topique de tissu thyroïdien ectopique ou de goitre rétrosternal. | DANS | |
| Dans les régions carencées en iode, la scintigraphie thyroïdienne pour MUT est indiquée même si le taux de TSH se situe dans la limite inférieure de la normale. | AVEC | |
| Tomodensitométrie | Ces méthodes permettent de diagnostiquer le goitre sous-sternal, de clarifier l'emplacement du goitre par rapport aux tissus environnants, de déterminer le déplacement ou la compression de la trachée et de l'œsophage. |
DANS |
| Imagerie par résonance magnétique | ||
| Examen radiologique avec contraste baryté de l'œsophage | ||
| Examen cytologique TAB |
Elles sont réalisées en présence de ganglions dans la glande thyroïde. Une biopsie par ponction est indiquée pour tous les nodules palpables ; Le risque de cancer est le même pour la formation nodulaire solitaire et le goitre multinodulaire. Avec les néoplasmes de la glande thyroïde, des cellules cancéreuses sont détectées. Dans AIT - infiltration lymphocytaire. |
DANS |
Tableau 6. Méthodes de diagnostic supplémentaires pour la thyréotoxicose :
| Type d'étude | Note | Probabilité de nomination |
| ECG | Diagnostic des troubles du rythme | 100% |
| Moniteur Holter ECG 24 heures sur 24 | Diagnostic des troubles cardiaques | 70% |
| Radiographie thoracique/fluorographie | Exclusion d'un processus spécifique lors du développement de CHF | 100% |
| Échographie des organes abdominaux | En présence d'ICC, lésions hépatiques toxiques | 50% |
| ECHO-cardiographie | En présence de tachycardie | 90% |
| EGDS | En présence d'une pathologie concomitante | 50% |
| Densitométrie | Diagnostic de l'ostéoporose | 50% |
Tableau 7. Indications de consultation spécialisée :
· consultation avec un neurologue/épileptologue - diagnostic différentiel avec épilepsie ;
· consultation avec un cardiologue - en cas de développement d'un « cœur thyrotoxique », d'ICC, d'arythmie ;
· consultation avec un ophtalmologiste - en combinaison avec un amplificateur de brillance pour évaluer la fonction du nerf optique, évaluer le degré d'exophtalmie, identifier les troubles du fonctionnement des muscles extraoculaires ;
· consultation avec un chirurgien - pour résoudre la question du traitement chirurgical ;
· consultation avec un oncologue - en présence d'un processus malin ;
· consultation d'un allergologue - si des effets secondaires se développent sous forme de manifestations cutanées lors de la prise de thyréostatiques ;
· consultation d'un gastro-entérologue - en cas de développement d'effets secondaires lors de la prise de thyréostatiques, en présence de myxœdème prétibial ;
· consultation avec un obstétricien-gynécologue - pendant la grossesse ;
· consultation avec un hématologue - si une agranulocytose se développe.
Algorithme de diagnostic :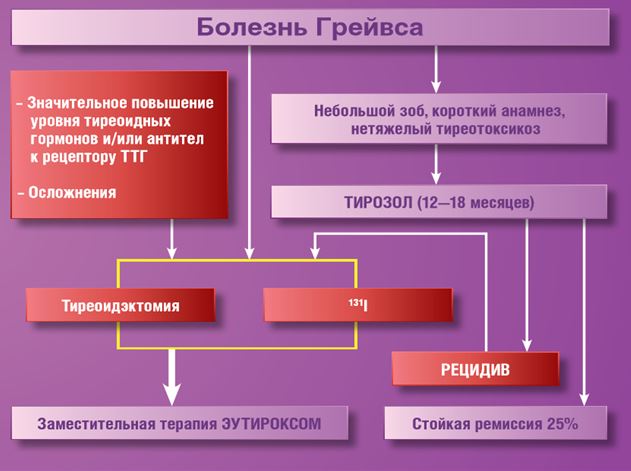
Diagnostic différentiel
Diagnostic différentiel
Tableau 8. Diagnostic différentiel de la thyréotoxicose :
| Diagnostic | En faveur du diagnostic |
| Maladie de Graves | Modifications diffuses sur le scintigramme, augmentation des taux d'anticorps anti-TPO, présence d'un amplificateur de brillance et myxœdème prétibial |
| Goitre toxique multinodulaire | Hétérogénéité du cliché scintigraphique |
| Nœuds chauds autonomes | Lésion « chaude » au scanogramme |
| Thyroïdite subaiguë de Quervain | La glande thyroïde n'est pas visualisée sur le scanogramme, taux élevés d'ESR et de thyroglobuline, syndrome douloureux |
| Thyrotoxicose iatrogène, Thyrotoxicose induite par l'amiodarone | Antécédents de prise d'interféron, de lithium ou de médicaments contenant de grandes quantités d'iode (amiodarone) |
| Adénome hypophysaire producteur de TSH | Augmentation du taux de TSH, absence de réponse de la TSH à la stimulation par la thyrolibérine |
| Choriocarcinome | Augmentation des niveaux de gonadotrophine chorionique humaine |
| Métastases du cancer de la thyroïde | Dans la plupart des cas, il y a eu une thyroïdectomie antérieure |
| Thyrotoxicose subclinique | L'absorption d'iode par la thyroïde peut être normale |
| Rechute de thyréotoxicose | Après le traitement HD |
| Struma ovarii - tératome ovarien contenant du tissu thyroïdien, accompagné d'hyperthyroïdie | augmentation de l'absorption des radiotraceurs dans la région pelvienne pendant l'examen du corps entier |
De plus, un diagnostic différentiel est réalisé avec des conditions similaires en termes de tableau clinique à la thyréotoxicose et des cas de suppression des taux de TSH sans thyréotoxicose :
· états d'anxiété;
· phéochromocytome;
· le syndrome pathologique euthyroïdien (suppression des taux de TSH dans les pathologies somatiques non thyroïdiennes sévères) ne conduit pas au développement d'une thyréotoxicose.
Traitement à l'étranger
Faites-vous soigner en Corée, en Israël, en Allemagne et aux États-Unis
Obtenez des conseils sur le tourisme médical
Traitement
Médicaments (ingrédients actifs) utilisés dans le traitement
Groupes de médicaments selon ATC utilisés dans le traitement
Traitement (clinique externe)
TACTIQUES DE TRAITEMENT AU NIVEAU EXTERNE : les patients atteints de la maladie de Basedow préalablement diagnostiquée sans décompensation de la maladie, qui ne nécessitent pas de thérapie à l'iode radioactif, de traitement chirurgical et sans crise thyréotoxique, sont soumis à un traitement ambulatoire .
Traitement non médicamenteux :
· Mode: dépend de la gravité de l'affection et de la présence de complications. Évitez l'activité physique, car avec la thyréotoxicose, la faiblesse musculaire et la fatigue augmentent, la thermorégulation est perturbée et la charge sur le cœur augmente.
· Régime: jusqu'à ce que l'euthyroïdie soit établie, il faut limiter l'apport d'iode dans l'organisme avec des produits de contraste, car L'iode contribue dans la plupart des cas au développement de la thyréotoxicose. La caféine doit être évitée car... la caféine peut augmenter les symptômes de la thyréotoxicose.
Traitement médical:
Thérapie thyréostatique conservatrice:
Pour supprimer la production d'hormones thyroïdiennes par la glande thyroïde, il est nécessaire d'utiliser thiamazole. Le thiamazole est utilisé à une dose quotidienne de 20 à 40 mg. En cas d'hyperthyroïdie clinique et biochimique sévère, les doses peuvent être augmentées de 50 à 100 %. Schéma posologique - généralement 2 à 3 fois par jour, il est permis de prendre le médicament une fois par jour.
Effets secondaires possibles de la thérapie thyréostatique : réactions allergiques, pathologie hépatique (1,3 %), agranulocytose (0,2 - 0,4 %). En cas d'apparition de fièvre, d'arthralgie, d'ulcères sur la langue, de pharyngite ou de malaise grave, l'utilisation de thyréostatiques doit être immédiatement arrêtée et un leucogramme élargi doit être déterminé. La durée du traitement conservateur par thyréostatiques est de 12 à 18 mois.
*
La TSH reste supprimée pendant une longue période (jusqu'à 6 mois) lors du traitement de la thyréotoxicose. Par conséquent, la détermination du niveau de TSH n’est pas utilisée pour ajuster la dose de thyréostatique. Le premier contrôle des taux de TSH est effectué au plus tôt 3 mois après l'obtention de l'euthyroïdie.
La dose de l'agent thyréostatique doit être ajustée en fonction du taux de T4 libre. Le premier contrôle de T4 libre est prescrit 3 à 4 semaines après le début du traitement. La dose de l'agent thyréostatique est réduite à une dose d'entretien (7,5 à 10 mg) après avoir atteint un niveau normal de T4 libre. Ensuite, la T4 libre est surveillée une fois toutes les 4 à 6 semaines en utilisant le régime « Bloquer » et une fois tous les 2-3 mois en utilisant le régime « Bloquer et remplacer » (lévothyroxine 25-50 mcg) à des doses adéquates.
Avant d'arrêter le traitement thyréostatique, il est conseillé de déterminer le niveau anticorps contre le récepteur TSH, car cela aide à prédire l'issue du traitement : les patients présentant de faibles taux d'AT-rTSH ont plus de chances d'obtenir une rémission stable.
La plupart des patients ayant une fréquence cardiaque au repos supérieure à 100 battements par minute ou souffrant d'une maladie cardiovasculaire sous-jacente doivent être traités par β-bloquants pendant 3 à 4 semaines (anapriline 40 à 120 mg/jour, aténolol 100 mg/jour, bisoprolol 2,5 à 10 mg/jour).
En association avec l'EOP et la présence de symptômes d'insuffisance surrénalienne, recourir à corticothérapie: prednisolone 10-15 mg ou hydrocortisone 50-75 mg par voie intramusculaire.
Traitement de la thyréotoxicose pendant la grossesse :
Si un taux de TSH supprimé est détecté au cours du premier trimestre (inférieur à 0,1 mU/l), il est nécessaire de déterminer les taux de fT4 et de fT3 chez tous les patients. Le diagnostic différentiel de la MG et de la thyréotoxicose gestationnelle repose sur la détection du goitre, des anticorps anti-rTSH, EOP ; la détection des anticorps anti-TPO ne permet pas de le faire (niveau B). La scintigraphie thyroïdienne est absolument contre-indiquée. Le traitement de choix de la thyréotoxicose pendant la grossesse est médicaments antithyroïdiens.
Le PTU et le thiamazole pénètrent librement dans la barrière placentaire, pénètrent dans le sang fœtal et peuvent provoquer le développement d'une hypothyroïdie et d'un goitre ainsi que la naissance d'un enfant dont l'intelligence est réduite. Par conséquent, les thyréostatiques sont prescrits aux doses les plus faibles possibles, suffisantes pour maintenir les hormones thyroïdiennes à un niveau 1,5 fois supérieur à celui des femmes non enceintes et la TSH en dessous du niveau typique des femmes enceintes. La dose de thiamazole ne doit pas dépasser 15 mg par jour, la dose de propylthiouracile* - 200 mg par jour.
La surveillance FT4 est effectuée après 2 à 4 semaines. Après avoir atteint le niveau cible de fT4, la dose de l'agent thyréostatique est réduite à un niveau d'entretien (thiamazole à 5-7,5 mg, propicil à 50-75 mg). Les niveaux de FT4 doivent être surveillés mensuellement. À la fin des deuxième et troisième trimestres, en raison d'une immunosuppression accrue, une rémission immunologique de la DG se produit et chez la plupart des femmes enceintes, le médicament thyréostatique est annulé.
Médicament de choix au premier trimestre, il y a une école professionnelle, dans les deuxième et troisième - thiamazole (niveau C). Cela est dû au fait que la prise de thiamazole dans des cas isolés peut être associée à des anomalies congénitales qui se développent pendant la période d'organogenèse au cours du premier trimestre. Si la PTU n'est pas disponible et intolérable, le thiamazole peut être prescrit. Chez les patientes recevant du thiamazole, si une grossesse est suspectée, il est nécessaire d'effectuer un test de grossesse le plus tôt possible et, en cas de grossesse, de les transférer vers la prise de PTU et, au début du deuxième trimestre, de reprendre la prise de thiamazole.
Si la patiente a initialement reçu du PTU, il est également recommandé de la faire passer au thiamazole au début du deuxième trimestre.
Utiliser un schéma de blocage et de remplacement contre-indiqué pendant la grossesse(Niveau A). Le régime « bloquer et remplacer » implique l'utilisation de doses plus élevées de médicaments thyréostatiques, ce qui peut conduire au développement d'une hypothyroïdie et d'un goitre chez le fœtus.
En cas de thyréotoxicose sévère et de nécessité de prendre de fortes doses d'antithyroïdiens, ainsi que d'intolérance aux thyréostatiques (réactions allergiques ou leucopénie sévère) ou refus de la femme enceinte de prendre des thyréostatiques, un traitement chirurgical est indiqué qui peut être réalisé au deuxième trimestre (niveau C).
Tableau 9. Traitement de la maladie de Basedow chez la femme enceinte :
| Temps de diagnostic | Caractéristiques de la situation | Recommandations |
| DG diagnostiquée pendant la grossesse | DG diagnostiquée au premier trimestre |
Commencez à prendre du Propylthiouracile*. |
| DG diagnostiquée après le premier trimestre |
Commencez à prendre du thiamazole. Mesurez le titre d'anticorps contre la rTSH s'il est élevé, répétez à 18-22 semaines et 30-34 semaines. Si une thyroïdectomie est nécessaire, le moment optimal est le deuxième trimestre. |
|
| DG diagnostiquée avant la grossesse | Prendre du thiamazole |
Passez au Propylthiouracile* ou arrêtez les thyréostatiques dès que le test de grossesse est confirmé. Mesurez le titre d'anticorps contre la rTSH s'il est élevé, répétez à 18-22 semaines et 30-34 semaines. |
| En rémission après arrêt des thyréostatiques. | Déterminez la fonction thyroïdienne pour confirmer l’euthyroïdie. Ne mesurez pas le titre AT en rTSH. | |
| A reçu un traitement à l'iode radioactif ou a subi une thyroïdectomie | Mesurez le titre d'anticorps contre la rTSH au cours du premier trimestre s'il est élevé, répétez à 18-22 semaines ; |
Après une thyroïdectomie ou une résection extrêmement subtotale de la glande thyroïde, un traitement substitutif par la lévothyroxine est prescrit à raison de 2,3 mcg/kg de poids corporel.
Réalisation thérapie à l'iode radioactif femmes enceintes contre-indiqué. Si I 131 est prescrit par inadvertance à une femme enceinte, celle-ci doit être informée du risque radiologique, y compris du risque de destruction de la thyroïde fœtale si I 131 I est pris après 12 semaines de grossesse. Il n’existe aucune recommandation pour ou contre l’interruption d’une grossesse au cours de laquelle une femme a reçu du 131 I.
En cas de diminution transitoire des taux de TSH induite par l'hCG en début de grossesse, les thyréostatiques ne sont pas prescrits.
Lorsqu'une thyréotoxicose est détectée chez une femme en période post-partum, il est nécessaire de réaliser un diagnostic différentiel entre DG et thyroïdite post-partum. Pour les femmes présentant des symptômes sévères de la phase thyréotoxique de la thyroïdite post-partum, des bêtabloquants peuvent être recommandés.
Traitement de la thyréotoxicose médicamenteuse :
Pour le traitement des manifestations induit par l'iode Pour la thyréotoxicose, les β-bloquants sont utilisés en monothérapie ou en association avec le thiamazole.
Chez les patients chez lesquels une thyréotoxicose s'est développée au cours du traitement l'interféron-α ou l'interleukine-2, un diagnostic différentiel entre la MG et la thyroïdite induite par les cytokines est nécessaire.
Pendant la thérapie amiodarone Une évaluation de la fonction thyroïdienne est recommandée avant, 1 et 3 mois après le début du traitement, puis à intervalles de 3 à 6 mois. La décision d'arrêter de prendre l'amiodarone dans le contexte d'une thyréotoxicose sévère doit être prise individuellement, sur la base de la consultation d'un cardiologue et de la présence ou de l'absence d'un traitement antiarythmique alternatif efficace. Le thiamazole doit être utilisé pour le traitement de la thyrotoxicose induite par l'amiodarone de type 1, et les glucocorticostéroïdes pour le traitement de la thyrotoxicose induite par l'amiodarone de type 2. En cas de thyréotoxicose sévère induite par l'amiodarone, qui ne répond pas à la monothérapie, ainsi que dans les situations où le type de maladie ne peut être déterminé avec précision, une association de thyréostatiques et de glucocorticoïdes est indiquée. Chez les patients atteints de thyréotoxicose induite par l'amiodarone qui ne répondent pas à un traitement combiné agressif avec le thiamazole et la prednisolone, une thyroïdectomie doit être réalisée.
Approches du traitement de la MH chez les patients atteints d'ophtalmopathie endocrinienne :
Le traitement thyréostatique chez les patients atteints de GD et d'EOP est réalisé de préférence selon le schéma « bloquer et remplacer » (niveau C). Il est recommandé de réaliser un traitement chirurgical de la DG en association avec un amplificateur de brillance à hauteur d'une thyroïdectomie totale afin de prévenir la progression d'un amplificateur de brillance en période postopératoire (niveau B).
Tous les patients atteints de GD et d'EOP nécessitent une correction médicamenteuse obligatoire de l'hypothyroïdie postopératoire dès le 1er jour après la chirurgie, suivie d'une détermination régulière des taux de TSH au moins une fois par an.
La thérapie à l'iode radioactif peut être recommandée comme méthode sûre de traitement de la thyréotoxicose en MH chez les patients atteints d'EOP, qui n'entraîne pas une aggravation de son évolution, à condition qu'un état euthyroïdien stable soit atteint dans la période post-irradiation dans le contexte d'un remplacement par la lévothyroxine. thérapie (niveau C).
Lors de la planification d'un traitement chirurgical ou d'une RIT de la MH, il est nécessaire de prendre en compte degré d'activité de l'intensificateur d'image. Pour les patients avec une phase inactive de l'intensificateur d'image (CAS)<3) предварительная подготовка не требуется, назначается только симптоматическое лечение (уровень А). В активную фазу (CAS≥5) до проведения хирургического лечения или РЙТ необходимо лечение глюкокортикоидами (уровень В). При низкой активности процесса (CAS=3-4) глюкокортикоиды назначаются, в основном, после радикального лечения. Пациентам с тяжелой степенью ЭОП и угрозой потери зрения проведение Le RHT est contre-indiqué. Les patients atteints de MH et d'EOP doivent arrêter de fumer et réduire leur poids (niveau B).
Liste des médicaments essentiels (ayant une probabilité d'utilisation de 100 %) :
Tableau 9. Médicaments utilisés pour traiter la MH :
| Groupe pharmacologique | Dénomination commune internationale du médicament |
Mode d'application |
Niveau de preuve |
| Médicament antithyroïdien |
Thiamazole H03BB02 |
Comprimés 5 et 10 mg par voie orale, dose quotidienne 10-40 mg (1-3 doses) | DANS |
| Propylthiuracile* H03BA02 | Comprimés 50 mg par voie orale, dose quotidienne 300-400 mg (pour 3 prises) | ||
| β-bloquants | |||
| Non sélectif (β1, β2) | Propranolol C07AA05 | Par voie orale 10 à 40 mg 3 à 4 fois par jour | DANS |
| Cardiosélectif (β1) |
Aténolol C07AB03 |
Comprimés par voie orale, 25 à 100 mg 1 à 2 fois par jour | DANS |
Liste des médicaments supplémentaires (probabilité d'utilisation inférieure à 100 %) :
Tableau 10. Médicaments utilisés pour l'insuffisance surrénalienne :
* postuler après l'enregistrement sur le territoire de la République du Kazakhstan
Intervention chirurgicale: Non.
Gestion complémentaire[4-6]:
· Une surveillance des patients recevant un traitement thyréostatique est effectuée pour la détection précoce des effets secondaires, tels qu'une éruption cutanée, une pathologie hépatique, une agranulocytose. Il est nécessaire d'étudier les taux de fT4 et de TSH toutes les 4 semaines pour une détection précoce de l'hypothyroïdie et la prescription d'un traitement substitutif. Dans l'année qui suit l'euthyroïdie, une évaluation en laboratoire de la fonction thyroïdienne est effectuée une fois tous les 3 à 6 mois, puis tous les 6 à 12 mois.
· Chez la femme enceinte avec la HD, il est nécessaire d'utiliser les doses les plus faibles de thyréostatiques, garantissant l'atteinte de taux d'hormones thyroïdiennes légèrement supérieurs à la plage de référence, avec suppression de la TSH. La fonction thyroïdienne pendant la grossesse doit être évaluée mensuellement et la dose d'agent thyréostatique ajustée si nécessaire.
Après une thérapie à l'iode radioactifje 131 La fonction thyroïdienne diminue progressivement. Surveillance des niveaux de TSH - tous les 3 à 6 mois. L'hypothyroïdie se développe généralement 2 à 3 mois après le traitement et, lorsqu'elle est détectée, la lévothyroxine doit être prescrite immédiatement.
Après une thyroïdectomie Concernant la HD il est recommandé :
· arrêter de prendre des médicaments antithyroïdiens et des ẞ-bloquants ;
· commencer à prendre de la lévothyroxine à une dose quotidienne correspondant au poids corporel du patient (1,6-1,8 mcg/kg), 6 à 8 semaines après le début de la lévothyroxine, déterminer le taux de TSH et, si nécessaire, ajuster la dose (la prise de lévothyroxine est un remplacement à vie traitement, les niveaux de TSH doivent être déterminés au moins 2 à 3 fois par an);
· dans les premiers jours après l'intervention chirurgicale, il est nécessaire de déterminer le taux de calcium (calcium libre de préférence) et de PTH et, si nécessaire, de prescrire une supplémentation en calcium et en vitamine D.
· Pour l'hypoparathyroïdie, la principale méthode de traitement consiste à préparer des préparations de vitamine D hydroxylée (alfacalcidol, calcitriol). La dose est choisie strictement individuellement en fonction du taux de calcium dans le sérum, qui est déterminé une fois tous les 3 jours. La dose initiale du médicament dépend du niveau de calcium libre (moins de 0,8 mmol/l : 1-1,5 mcg/jour ; 0,8-1,0 mmol/l : 0,5-1 mcg/jour).
Il n'y a aucune restriction quant à la dose minimale ou maximale de vitamine D. Le critère pour une dose adéquate est un taux de calcium ionisé ne dépassant pas 1,2 mmol/l pendant 10 jours ; après avoir sélectionné une dose adéquate, les niveaux de calcium sont surveillés en continu toutes les 2 à 4 semaines et, si nécessaire, la dose du médicament est ajustée. De plus, des suppléments de calcium sont prescrits à une dose de 500 à 3 000 mg/jour pour garantir une quantité suffisante de calcium. apport dans le corps.
Les patients ayant subi une thyroïdectomie et recevant un traitement substitutif par la lévothyroxine doivent ensuite être surveillés de la manière habituelle comme pour les patients souffrant d'hypothyroïdie (hypoparathyroïdie).
Après un traitement I 131 ou un traitement chirurgical, le patient doit être surveillé toute sa vie en relation avec le développement de l'hypothyroïdie.
Indicateurs d'efficacité du traitement :
· réduction ou élimination des symptômes de la thyréotoxicose, permettant au patient d'être transféré en traitement ambulatoire ;
Réduire la taille du goitre ;
· réduire la dose de thyréostatiques nécessaire au maintien de l'euthyroïdie ;
· disparition ou diminution de la teneur en anticorps dirigés contre les récepteurs TSH.
Traitement (hospitalisé)
TACTIQUES DE TRAITEMENT AU NIVEAU DES PATIENTS HOMOLOGIQUES : les patients présentant une thyréotoxicose nouvellement diagnostiquée, pour une thérapie à l'iode radioactif et un traitement chirurgical, ainsi qu'en état de décompensation et de crise thyréotoxique, sont soumis à un traitement hospitalier .
Carte d'observation des patients, acheminement des patients
Traitement non médicamenteux : voir niveau ambulatoire.
Thérapie à l'iode radioactif :
Les indicationsà la thérapie à l'iode radioactif sont :
· rechute postopératoire de thyréotoxicose ;
· évolution récurrente de la thyréotoxicose au cours du traitement par thyréostatiques ;
· intolérance aux thyréostatiques.
Chez les patients atteints de MG qui n'ont pas développé de rémission de la maladie 1 à 2 ans après le traitement au thiamazole, un traitement par iode radioactif ou une thyroïdectomie doit être envisagé.
Chez les personnes atteintes de thyréotoxicose sévère, lorsque le taux de T4 total est > 20 μg/dL (260 nmol/L) ou que le taux de FT4 est > 5 ng/dL (60 pmol/L), le thiamazole et les β-bloquants doivent être prescrits avant de 131 thérapie afin de normaliser ces indicateurs. Le traitement médicamenteux par thyréostatiques est généralement arrêté 10 jours avant la nomination de l'I 131 (en cas de thyréotoxicose sévère, il est possible d'arrêter le traitement 3 à 5 jours avant). Les agents thyréostatiques ne sont pas arrêtés avant un traitement à l'iode radioactif chez les patients présentant une thyréotoxicose sévère et/ou un goitre volumineux afin de prévenir une crise thyréotoxique.
Traitement médical: voir niveau ambulatoire.
Crise thyrotoxique (TC)- une maladie rare caractérisée par une atteinte multisystémique et une mortalité dans 8 à 25 % des cas. Critères de diagnostic TC - critères de diagnostic unifiés (échelle BWPS).
Tous les patients atteints de TC nécessitent une observation en unité de soins intensifs et toutes les fonctions vitales doivent être surveillées. Le traitement doit être instauré immédiatement, sans attendre les résultats d'un test sanguin hormonal. 
Tableau 11. Traitement de la crise thyréotoxique:
| MP | Dose |
Un goitre simple non toxique, qui peut être diffus ou nodulaire, est une hypertrophie non néoplasique de la glande thyroïde sans développer d'état d'hyperthyroïdie, d'hypothyroïdie ou d'inflammation. La cause est généralement inconnue, mais on pense qu'elle pourrait être le résultat d'une hyperstimulation prolongée par la thyréostimuline, le plus souvent en réponse à une carence en iode (goitre colloïde endémique) ou à la prise de divers composants alimentaires ou de médicaments qui inhibent la synthèse. des hormones thyroïdiennes. Sauf en cas de carence sévère en iode, la fonction thyroïdienne est normale et les patients sont asymptomatiques avec une glande thyroïde dense et hypertrophiée. Le diagnostic repose sur l'examen clinique et la confirmation en laboratoire de la fonction thyroïdienne normale. Les mesures thérapeutiques visent à éliminer la cause principale de la maladie ; en cas de développement d'un goitre trop volumineux, un traitement chirurgical (thyroïdectomie partielle) est préférable.
, , , ,
Code CIM-10
E04.0 Goitre diffus non toxique
Causes du goitre simple non toxique (goitre euthyroïdien)
Le goitre simple non toxique est la cause la plus courante et la plus typique d'hypertrophie de la glande thyroïde, le plus souvent détecté pendant la puberté, la grossesse et la ménopause. La raison n’est pas encore claire dans la plupart des cas. Les causes connues sont des défauts établis dans la production d'hormones thyroïdiennes dans l'organisme et une carence en iode dans certains pays, ainsi que la consommation d'aliments contenant des composants qui suppriment la synthèse des hormones thyroïdiennes (appelés goitrogènes, par exemple le chou, le brocoli, le chou-fleur). , manioc). D'autres causes connues sont dues à l'utilisation de médicaments qui réduisent la synthèse des hormones thyroïdiennes (par exemple, l'amiodarone ou d'autres médicaments contenant de l'iode, le lithium).
La carence en iode est rare en Amérique du Nord, mais reste l’une des principales causes d’épidémies de goitre dans le monde (appelée goitre endémique). De faibles augmentations compensatoires de la TSH sont observées, empêchant le développement de l'hypothyroïdie, mais la stimulation de la TSH elle-même plaide en faveur d'un goitre nodulaire non toxique. Cependant, la véritable étiologie de la plupart des goitres non toxiques survenant dans les régions où l’iode est suffisante est inconnue.
, , , ,
Symptômes du goitre simple non toxique (goitre euthyroïdien)
Les patients peuvent avoir des antécédents de faible apport alimentaire en iode ou d’apport alimentaire élevé en goitrogènes, mais ce phénomène est rare en Amérique du Nord. Aux premiers stades, l’hypertrophie de la glande thyroïde est généralement molle et lisse, et les deux lobes sont symétriques. Plus tard, plusieurs ganglions et kystes peuvent se développer.
L'accumulation d'iode radioactif dans la glande thyroïde est déterminée, une analyse et une détermination des indicateurs de laboratoire de la fonction thyroïdienne (T3, T4, TSH) sont effectuées. Aux stades précoces, l’accumulation d’iode radioactif par la glande thyroïde peut être normale ou élevée avec une image scintigraphique normale. Les valeurs de laboratoire sont généralement normales. Les anticorps dirigés contre le tissu thyroïdien sont testés pour les différencier de la thyroïdite de Hashimoto.
Dans le goitre endémique, la TSH sérique peut être légèrement élevée et la T3 sérique à la limite inférieure de la normale ou légèrement diminuée, mais les taux sériques de T3 sont généralement normaux ou légèrement élevés.
Traitement du goitre simple non toxique (goitre euthyroïdien)
Dans les régions déficitaires en iode, l'iodation du sel est utilisée ; administration orale ou intramusculaire de solutions d'huile iodée chaque année ; L'iodation de l'eau, des céréales ou l'utilisation d'aliments pour animaux (fourrage) réduit l'incidence du goitre dû à une carence en iode. La consommation de composants goitrogènes doit être évitée.
Dans d'autres régions, on utilise la suppression de la zone hypothalamo-hypophysaire avec des hormones thyroïdiennes, bloquant la production de TSH (d'où la stimulation de la glande thyroïde). Les doses de L-thyroxine suppressives de la TSH nécessaires pour la supprimer complètement (100 à 150 mcg/jour par voie orale, en fonction des taux sériques de TSH) sont particulièrement efficaces chez les jeunes patients. L'utilisation de L-thyroxine est contre-indiquée chez les personnes âgées et séniles atteintes de goitres nodulaires non toxiques, car ces types de goitres diminuent rarement en taille et peuvent contenir des zones à fonction autonome (non dépendante de la TSH), auquel cas la prise de L- la thyroxine peut conduire au développement d'un état hyperthyroïdien. Les patients atteints de gros goitre nécessitent souvent une intervention chirurgicale ou un traitement à l'iode radioactif (131-I) pour réduire suffisamment la taille de la glande afin de prévenir l'apparition de difficultés respiratoires ou de déglutition ou de problèmes associés à une correction esthétique.
Il est important de le savoir !
La vascularisation de la glande thyroïde peut être évaluée à l’aide du flux coloré et de l’échographie Doppler pulsée. Selon le problème clinique (maladie thyroïdienne diffuse ou focale), le but de l'étude peut être de quantifier la vascularisation de la glande thyroïde ou de déterminer sa structure vasculaire.
Classe IV. Maladies du système endocrinien, troubles nutritionnels et troubles métaboliques (E00-E90)
Note. Tous les néoplasmes (fonctionnellement actifs et inactifs) sont inclus dans la classe II. Les codes correspondants de cette classe (par exemple, E05.8, E07.0, E16-E31, E34. -) peuvent, si nécessaire, être utilisés comme codes supplémentaires pour identifier les néoplasmes fonctionnellement actifs et le tissu endocrinien ectopique, ainsi que l'hyperfonctionnement. et hypofonctionnement des glandes endocrines, associés à des néoplasmes et à d'autres troubles classés ailleurs.
Exclus : complications de la grossesse, de l'accouchement et du post-partum (O00-O99), symptômes, signes et anomalies identifiés lors d'essais cliniques et de laboratoire, non classés ailleurs (R00-R99), troubles endocriniens et troubles métaboliques transitoires, spécifiques du fœtus et du nouveau-né. (P70-P74)
Cette classe contient les blocs suivants :
E00-E07 Maladies de la glande thyroïde
E10-E14 Diabète sucré
E15-E16 Autres troubles de la régulation du glucose et du système endocrinien pancréatique
E20-E35 Troubles d'autres glandes endocrines
E40-E46 Malnutrition
E50-E64 Autres types de malnutrition
E65-E68 Obésité et autres types de nutrition excessive
E70-E90 Troubles métaboliques
Les catégories suivantes sont indiquées par un astérisque :
E35 Troubles des glandes endocrines lors de maladies classées ailleurs
E90 Troubles alimentaires et métaboliques dans les maladies classées ailleurs
MALADIES DE LA THYROÏDE (E00-E07)
E00 Syndrome de carence congénitale en iode
Inclus : les conditions endémiques associées à la carence en iode dans l'environnement naturel, à la fois directement et
et en raison d’une carence en iode dans le corps de la mère. Certaines de ces affections ne peuvent pas être considérées comme une véritable hypothyroïdie, mais sont la conséquence d'une sécrétion insuffisante d'hormones thyroïdiennes chez le fœtus en développement ; il peut y avoir un lien avec des facteurs goitrogènes naturels. Si nécessaire, identifiez le retard mental concomitant, utilisez un code supplémentaire (F70-F79).
À l'exclusion de : hypothyroïdie subclinique due à une carence en iode (E02)
E00.0 Syndrome de carence congénitale en iode, forme neurologique. Crétinisme endémique, forme neurologique
E00.1 Syndrome de carence congénitale en iode, forme myxœdème.
Crétinisme endémique :
. hypothyroïdie
. forme de myxœdème
E00.2 Syndrome de carence congénitale en iode, forme mixte.
Crétinisme endémique, forme mixte
E00.9 Syndrome de carence congénitale en iode, sans précision.
Hypothyroïdie congénitale par carence en iode SAI. Crétinisme endémique SAI
E01 Maladies thyroïdiennes associées à une carence en iode et affections associées
A l'exclusion de : syndrome de carence congénitale en iode (E00.-)
hypothyroïdie subclinique due à une carence en iode (E02)
E01.0 Goitre diffus (endémique) associé à une carence en iode
E01.1 Goitre multinodulaire (endémique) associé à une carence en iode. Goitre nodulaire associé à une carence en iode
E01.2 Goitre (endémique), associé à une carence en iode, sans précision. Goitre endémique SAI
E01.8 Autres maladies thyroïdiennes associées à une carence en iode et à des conditions similaires.
Hypothyroïdie acquise par carence en iode SAI
E02 Hypothyroïdie subclinique due à une carence en iode
E03 Autres formes d'hypothyroïdie
À l'exclusion de : hypothyroïdie associée à une carence en iode (E00-E02)
hypothyroïdie suite à une intervention médicale (E89.0)
E03.0 Hypothyroïdie congénitale avec goitre diffus.
Goitre (non toxique) congénital :
. SAI
. parenchyme
E03.1 Hypothyroïdie congénitale sans goitre. Aplasie de la glande thyroïde (avec myxœdème).
Congénital:
. atrophie thyroïdienne
. hypothyroïdie SAI
E03.2 Hypothyroïdie causée par des médicaments et d'autres substances exogènes.
Si nécessaire, identifiez la cause, utilisez un code supplémentaire de causes externes (classe XX).
E03.3 Hypothyroïdie post-infectieuse
E03.4 Atrophie de la glande thyroïde (acquise).
À l'exclusion de : atrophie congénitale de la glande thyroïde (E03.1)
E03.5 Coma myxœdème
E03.8 Autres hypothyroïdies précisées
E03.9 Hypothyroïdie, sans précision. Myxœdème SAI
E04 Autres formes de goitre non toxique
À l'exclusion de : goitre congénital :
. NSA)
. diffus ) (E03.0)
. parenchymateux)
goitre associé à une carence en iode (E00-E02)
E04.0 Goitre diffus non toxique.
Goitre non toxique :
. diffus (colloïdal)
. simple
E04.1 Goitre mononodulaire non toxique. Nœud colloïde (kystique) (thyroïde).
Goitre mononode non toxique. Nodule thyroïdien (kystique) SAI.
E04.2 Goitre multinodulaire non toxique. Goitre kystique SAI. Goitre polynodeux (kystique) SAI
E04.8 Autres formes spécifiées de goitre non toxique
E04.9 Goitre non toxique, sans précision. Goitre SAI. Goitre nodulaire (non toxique) SAI
E05 Thyrotoxicose [hyperthyroïdie]
À l'exclusion de : thyroïdite chronique avec thyréotoxicose transitoire (E06.2)
thyréotoxicose néonatale (P72.1)
E05.0 Thyrotoxicose avec goitre diffus. Exophtalmique ou toxique, appelez NOS. Maladie de Graves. Goitre toxique diffus
E05.1 Thyrotoxicose avec goitre uninodulaire toxique. Thyrotoxicose avec goitre mononode toxique
E05.2 Thyrotoxicose avec goitre multinodulaire toxique. Goitre nodulaire toxique SAI
E05.3 Thyrotoxicose avec ectopie du tissu thyroïdien
E05.4 Thyrotoxicose artificielle
E05.5 Crise thyroïdienne ou coma
E05.8 Autres formes de thyréotoxicose. Hypersécrétion d'hormone stimulant la thyroïde.
E05.9 Thyrotoxicose, sans précision. Hyperthyroïdie SAI. Cardiopathie thyréotoxique (I43.8)
E06 Thyroïdite
À l'exclusion de : thyroïdite post-partum (O90.5)
E06.0 Thyroïdite aiguë. Abcès de la glande thyroïde.
Thyroïdite :
. pyogène
. purulent
S'il est nécessaire d'identifier l'agent infectieux, un code supplémentaire (B95-B97) est utilisé.
E06.1 Thyroïdite subaiguë.
Thyroïdite :
. de Quervain
. cellule géante
. granulomateux
. non purulent
À l'exclusion de : thyroïdite auto-immune (E06.3)
E06.2 Thyroïdite chronique avec thyréotoxicose transitoire.
À l'exclusion de : thyroïdite auto-immune (E06.3)
E06.3 Thyroïdite auto-immune. Thyroïdite de Hashimoto. Chasitoxicose (transitoire). Goitre lymphadénomateux.
Thyroïdite lymphocytaire. Struma lymphomateux
E06.4 Thyroïdite d'origine médicamenteuse
E06.5 Thyroïdite :
. chronique:
. SAI
. fibreux
. boisé
. Riedel
E06.9 Thyroïdite, sans précision
E07 Autres maladies thyroïdiennes
E07.0 Hypersécrétion de calcitonine. Hyperplasie des cellules C de la glande thyroïde.
Hypersécrétion de thyrocalcitonine
E07.1 Goitre dysormonal. Goitre dyshormonal familial. Le syndrome de Pendred.
Exclus : goitre congénital transitoire avec fonction normale (P72.0)
E07.8 Autres maladies spécifiées de la glande thyroïde. Défaut de la globuline liant la tyrosine.
Hémorragie)
Infarctus) (c) de la ou des glandes thyroïde(s)
Syndrome d'euthyroïdie altérée
E07.9 Maladie thyroïdienne, sans précision
DIABÈTE SUCRÉ (E10-E14)
S'il est nécessaire d'identifier le médicament à l'origine du diabète, utilisez un code de cause externe supplémentaire (classe XX).
Les quatrièmes caractères suivants sont utilisés avec les catégories E10-E14 :
.0 Avec coma
Diabérique :
. coma avec ou sans acidocétose (acidocétose)
. coma hypersmolaire
. coma hypoglycémique
Coma hyperglycémique SAI
1 Avec acidocétose
Diabétique:
. acidose)
. acidocétose) sans mention de coma
2 Avec des lésions rénales
Néphropathie diabétique (N08.3)
Glomérulonéphrose intracapillaire (N08.3)
Syndrome de Kimmelstiel-Wilson (N08.3)
3 Avec des lésions oculaires
Diabétique:
. cataracte (H28.0)
. rétinopathie (H36.0)
4 Avec complications neurologiques
Diabétique:
. amyotrophie (G73.0)
. neuropathie autonome (G99.0)
. mononeuropathie (G59.0)
. polyneuropathie (G63.2)
. autonome (G99.0)
5 Avec des troubles circulatoires périphériques
Diabétique:
. gangrène
. angiopathie périphérique (I79.2)
. ulcère
6 Avec d'autres complications spécifiées
Arthropathie diabétique (M14.2)
. neuropathique (M14.6)
7 Avec de multiples complications
8 Avec complications non précisées
9 Aucune complication
E10 Diabète sucré insulino-dépendant
[cm. au-dessus des titres]
Inclus : diabète (sucré) :
. labile
. avec début à un jeune âge
. avec une tendance à la cétose
. tapez je
Exclus : diabète sucré :
. nouveau-nés (P70.2)
période (O24. -)
glycosurie :
. SAI (R81)
. rénal (E74.8)
E11 Diabète sucré non insulino-dépendant
Inclus : diabète (sucré) (non obèse) (obèse) :
. avec apparition à l'âge adulte
. sans tendance à la cétose
. écurie
. type II
Exclus : diabète sucré :
. associé à la malnutrition (E12.-)
. chez les nouveau-nés (P70.2)
. pendant la grossesse, pendant l'accouchement et après l'accouchement
période (O24. -)
glycosurie :
. SAI (R81)
. rénal (E74.8)
intolérance au glucose (R73.0)
hypoinsulinémie postopératoire (E89.1)
E12 Diabète sucré associé à la malnutrition
[cm. les sous-titres ci-dessus]
Comprend : diabète sucré associé à la malnutrition :
. insulino-dépendant
. non insulinodépendant
Exclus : diabète sucré pendant la grossesse, pendant l'accouchement
et dans la période post-partum (O24. -)
glycosurie :
. SAI (R81)
. rénal (E74.8)
intolérance au glucose (R73.0)
diabète sucré des nouveau-nés (P70.2)
hypoinsulinémie postopératoire (E89.1)
E13 Autres formes précisées de diabète sucré
[cm. les sous-titres ci-dessus]
Exclus : diabète sucré :
. insulino-dépendant (E10.-)
. associé à la malnutrition (E12.-)
. néonatal (P70.2)
. pendant la grossesse, pendant l'accouchement et après l'accouchement
période (O24. -)
glycosurie :
. SAI (R81)
. rénal (E74.8)
intolérance au glucose (R73.0)
hypoinsulinémie postopératoire (E89.1)
E14 Diabète sucré, sans précision
[cm. les sous-titres ci-dessus]
Inclus : diabète SAI
Exclus : diabète sucré :
. insulino-dépendant (E10.-)
. associé à la malnutrition (E12.-)
. nouveau-nés (P70.2)
. non insulinodépendant (E11.-)
. pendant la grossesse, pendant l'accouchement et après l'accouchement
période (O24. -)
glycosurie :
. SAI (R81)
. rénal (E74.8)
intolérance au glucose (R73.0)
hypoinsulinémie postopératoire (E89.1)
AUTRES TROUBLES DU GLUCOSE ET DE LA SÉCRÉTION INTERNE
PANCRÉAS (E15-E16)
E15 Coma hypoglycémique non diabétique. Coma insulinique non diabétique causé par des médicaments
moyens. Hyperinsulinisme avec coma hypoglycémique. Coma hypoglycémique SAI.
S'il est nécessaire d'identifier le médicament provoquant le coma hypolycémique non diabétique, utilisez un code de cause externe supplémentaire (classe XX).
E16 Autres troubles du système endocrinien pancréatique
E16.0 Hypoglycémie médicamenteuse sans coma.
S'il est nécessaire d'identifier le médicament, utilisez un code supplémentaire pour les causes externes (classe XX).
E16.1 Autres formes d'hypoglycémie. Hypoglycémie fonctionnelle non hyperinsulinémique.
Hyperinsulinisme :
. SAI
. fonctionnel
Hyperplasie des cellules bêta des îlots pancréatiques SAI. Encéphalopathie après coma hypoglycémique
E16.2 Hypoglycémie, sans précision
E16.3 Augmentation de la sécrétion de glucagon.
Hyperplasie des cellules des îlots pancréatiques avec hypersécrétion de glucagon
E16.8 Autres troubles précisés de la sécrétion interne du pancréas. Hypergastrinémie.
Hypersécrétion :
. hormone de libération de l'hormone de croissance
. polypeptide pancréatique
. somatostatine
. polypeptide intensinal vasoactif
Syndrome de Zollinger-Ellison
E16.9 Trouble du pancréas endocrinien, sans précision. Hyperplasie des cellules des îlots SAI.
Hyperplasie des cellules endocriniennes pancréatiques SAI
TROUBLES DES AUTRES GLANDES ENDOCRINES (E20-E35)
À l'exclusion de : galactorrhée (N64.3)
gynécomastie (N62)
E20 Hypoparathyroïdie
À l'exclusion de : syndrome de DiGeorge (D82.1)
hypoparathyroïdie suite à un acte médical (E89.2)
tétanie SAI (R29.0)
hypoparathyroïdie transitoire du nouveau-né (P71.4)
E20.0 Hypoparathyroïdie idiopathique
E20.1 Pseudohypoparathyroïdie
E20.8 Autres formes d'hypoparathyroïdie
E20.9 Hypoparathyroïdie, sans précision. Tétagie parathyroïdienne
E21 Hyperparathyroïdie et autres troubles de la glande parathyroïde [parathyroïde]
Exclut : ostéomalacie :
. chez l'adulte (M83.-)
. dans l'enfance et l'adolescence (E55.0)
E21.0 Hyperparathyroïdie primaire. Hyperplasie des glandes parathyroïdes.
Ostéodystrophie fibreuse généralisée [maladie osseuse de Recklinghausen]
E21.1 Hyperparathyroïdie secondaire, non classée ailleurs.
À l'exclusion de : hyperparathyroïdie secondaire d'origine rénale (N25.8)
E21.2 Autres formes d'hyperparathyroïdie.
À l'exclusion de : hypercalcémie hypocalciurique familiale (E83.5)
E21.3 Hyperparathyroïdie, sans précision
E21.4 Autres troubles parathyroïdiens précisés
E21.5 Maladie parathyroïdienne, sans précision
E22 Hyperfonctionnement de l'hypophyse
À l'exclusion de : syndrome d'Itsenko-Cushing (E24.-)
Syndrome de Nelson (E24.1)
hypersécrétion :
. hormone adrénocorticotrope [ACTH], non liée
avec le syndrome d'Itsenko-Cushing (E27.0)
. ACTH hypophysaire (E24.0)
. hormone stimulant la thyroïde (E05.8)
E22.0 Acromégalie et gigantisme hypophysaire.
Arthropathie associée à l'acromégalie (M14.5).
Hypersécrétion d'hormone de croissance.
Exclus : constitutionnels :
. gigantisme (E34.4)
. grand (E34.4)
hypersécrétion d'hormone de libération de l'hormone de croissance (E16.8)
E22.1 Hyperprolactinémie. S'il est nécessaire d'identifier le médicament provoquant l'hyperprolactinémie, utilisez un code de cause externe supplémentaire (classe XX).
E22.2 Syndrome de sécrétion inappropriée d'hormone antidiurétique
E22.8 Autres conditions d'hyperfonctionnement hypophysaire. Puberté précoce d'origine centrale
E22.9 Hyperfonctionnement hypophysaire, sans précision
E23 Hypofonction et autres troubles hypophysaires
Comprend : les affections répertoriées causées par des maladies de l'hypophyse et de l'hypothalamus.
À l'exclusion de : hypopituitarisme consécutif à une intervention médicale (E89.3)
E23.0 Hypopitutarisme. Syndrome eunuchoide fertile. Hypogonadisme hypogonadotrope.
Déficit idiopathique en hormone de croissance.
Panne isolée :
. gonadotrophine
. hormone de croissance
. autres hormones hypophysaires
syndrome de Kallmann
Petite taille [nanisme] Lorraine-Levy
Nécrose de l'hypophyse (post-partum)
Panhypopituitarisme
Pituitaire:
. cachexie
. Carence en SAI
. petite taille [nanisme]
Le syndrome de Sheehan. Maladie de Simmonds
E23.1 Hypopituitarisme d'origine médicamenteuse.
E23.2 Diabète insipide.
À l'exclusion de : diabète insipide néphrogénique (N25.1)
E23.3 Dysfonctionnement hypothalamique non classé ailleurs.
Exclut : syndrome de Prader-Willi (Q87.1), syndrome de Russell-Silver (Q87.1)
E23.6 Autres maladies de l'hypophyse. Abcès hypophysaire. Dystrophie adiposogénitale
E23.7 Maladie hypophysaire, sans précision
E24 Syndrome d'Itsenko-Cushing
E24.0 Maladie d'Itsenko-Cushing d'origine hypophysaire. Hypersécrétion d'ACTH par l'hypophyse.
Hypercorticisme d'origine hypophysaire
E24.1 Le syndrome de Nelson
E24.2 Syndrome d'Itsenko-Cushing d'origine médicamenteuse.
S'il est nécessaire d'identifier le médicament, utilisez un code supplémentaire pour les causes externes (classe XX).
E24.3 Syndrome d'ACTH ectopique
E24.4 Syndrome cushingoïde induit par l'alcool
E24.8 Autres conditions caractérisées par le syndrome cushingoïde
E24.9 Syndrome d'Itsenko-Cushing, sans précision
E25 Troubles surrénogénitaux
Comprend : syndromes surrénogénitaux, virilisation ou féminisation, acquis ou dus à une hyperplasie
glandes surrénales, conséquence de défauts congénitaux enzymatiques dans la synthèse des hormones
femelle:
. faux hermaphrodisme surrénalien
. fausse puberté prématurée hétérosexuelle
maturité
Pour des hommes:
. fausse puberté isosexuelle prématurée
maturité
. macrogénitosomie précoce
. puberté prématurée avec hyperplasie
glandes surrénales
. virilisation (femelle)
E25.0 Troubles surrénogénitaux congénitaux associés à un déficit enzymatique. Hyperplasie surrénale congénitale. Déficit en 21-hydroxylase. Hyperplasie surrénalienne congénitale entraînant une perte de sel
E25.8 Autres troubles surrénogénitaux. Trouble surrénogénital idiopathique.
Si nécessaire, identifiez le médicament à l'origine du trouble surrénogénital, utilisez le code de cause externe supplémentaire (classe XX).
E25.9 Trouble surrénogénital, sans précision. Syndrome surrénogénital SAI
E26 Hyperaldostéronisme
E26.0 Hyperaldostéronisme primaire. Le syndrome de Conn. aldostéronisme primaire provoqué par une hyperplasie du supra-
glandes rénales (bilatérales)
E26.1 Hyperaldostéronisme secondaire
E26.8 Autres formes d'hyperaldostéronisme. Syndrome de troc
E26.9 Hyperaldostéronisme, sans précision
E27 Autres troubles surrénaliens
E27.0 Autres types d'hypersécrétion du cortex surrénalien.
Hypersécrétion d'hormone adrénocorticotrope [ACTH], non associée à la maladie de Cushing.
À l'exclusion de : syndrome d'Itsenko-Cushing (E24.-)
E27.1 Insuffisance surrénalienne primaire. La maladie d'Addison. Inflammation auto-immune des glandes surrénales.
Exclus : amylose (E85.-), maladie d'Addison d'origine tuberculeuse (A18.7), syndrome de Waterhouse-Friderichsen (A39.1)
E27.2 La crise d'Addison. Crise surrénalienne. Crise corticosurrénalienne
E27.3 Insuffisance surrénalienne d'origine médicamenteuse. Si nécessaire, identifiez le médicament, utilisez un code supplémentaire pour les causes externes (classe XX).
E27.4 Insuffisance surrénalienne autre et non précisée.
Surrénal:
. saignement
. crise cardiaque
Suffisance du cortex surrénalien SAI. Hypoaldostéronisme.
Exclus : adrénoleucodystrophie [Addison-Schilder] (E71.3), syndrome de Waterhouse-Friderichsen (A39.1)
E27.5 Hyperfonctionnement de la médullosurrénale. Hyperplasie de la médullosurrénale.
Hypersécrétion de catécholamines
E27.8 Autres troubles surrénaliens spécifiés. Trouble des globulines liant le cortisol
E27.9 Maladie surrénalienne, sans précision
E28 Dysfonctionnement ovarien
Exclus : insuffisance gonadotrope isolée (E23.0)
insuffisance ovarienne suite à une intervention médicale (E89.4)
E28.0 Excès d’oestrogène. S'il est nécessaire d'identifier le médicament provoquant un excès d'œstrogènes, utilisez un code de cause externe supplémentaire (classe XX).
E28.1 Excès d'androgènes. Hypersécrétion d'androgènes ovariens. S'il est nécessaire d'identifier le médicament provoquant un excès d'androgènes, utilisez le code de cause externe supplémentaire (Classe XX).
E28.2 Syndrome des ovaires polykystiques. Syndrome des ovaires sclérokystiques. Syndrome de Stein-Leventhal
E28.3 Insuffisance ovarienne primaire. Faible teneur en œstrogènes. Ménopause prématurée SAI.
Syndrome ovarien persistant.
Exclut : la ménopause et l'état ménopausique de la femme (N95.1)
dysgénésie gonadique pure (Q99.1)
Syndrome de Turner (Q96.-)
E28.8 Autres types de dysfonctionnement ovarien. Hyperfonctionnement ovarien SAI
E28.9 Dysfonctionnement ovarien, sans précision
E29 Dysfonctionnement testiculaire
Azoospermie ou oligospermie SAI (N46)
insuffisance gonadotrope isolée (E23.0)
Syndrome de Klinefelter (Q98.0-Q98.2, Q98.4)
hypofonctionnement testiculaire suite à un acte médical (E89.5)
féminisation testiculaire (syndrome) (E34.5)
E29.0 Hyperfonctionnement des testicules. Hypersécrétion d'hormones testiculaires
E29.1 Hypofonction testiculaire. Trouble de la biosynthèse testiculaire des androgènes SAI
Déficit en 5-alpha réductase (avec pseudohermaphrodisme masculin). Hypogonadisme testiculaire SAI.
Si nécessaire, identifiez le médicament qui a provoqué l'hypofonctionnement des testicules, utilisez des
code de cause externe (classe XX).
E29.8 Autres types de dysfonctionnement testiculaire
E29.9 Dysfonctionnement testiculaire, sans précision
E30 Troubles de la puberté, non classés ailleurs
E30.0 Puberté retardée. Retard constitutionnel de la puberté.
Puberté retardée
E30.1 Puberté prématurée. Menstruations prématurées.
À l'exclusion de : syndrome d'Albright(-McCune)(-Sternberg) (Q78.1)
développement sexuel précoce d'origine centrale (E22.8)
fausse puberté prématurée féminine hétérosexuelle (E25. -)
fausse puberté prématurée isosexuelle masculine (E25. -)
E30.8 Autres troubles de la puberté. Thélarche prématurée
E30.9 Trouble de la puberté, sans précision
E31 Dysfonctionnement polyglandulaire
À l'exclusion de : ataxie télangiectasie [Louis-Bart] (G11.3)
dystrophie myotonique [Steinert] (G71.1)
pseudohypoparathyroïdie (E20.1)
E31.0 Déficit polyglandulaire auto-immun. Syndrome de Schmidt
E31.1 Hyperfonctionnement polyglandulaire.
À l'exclusion de : adénomatose endocrinienne multiple (D44.8)
E31.8 Autre dysfonctionnement polyglandulaire
E31.9 Dysfonctionnement polyglandulaire, sans précision
E32 Maladies du thymus
Exclus : aplasie ou hypoplasie avec déficit immunitaire (D82.1), myasthénie grave (G70.0)
E32.0 Hyperplasie persistante du thymus. Hypertrophie thymique
E32.1 Abcès du thymus
E32.8 Autres maladies du thymus
E32.9 Maladie du thymus, sans précision
E34 Autres troubles endocriniens
À l'exclusion de : pseudohypoparathyroïdie (E20.1)
E34.0 Syndrome carcinoïde.
Note. Si nécessaire, un code supplémentaire peut être utilisé pour identifier l'activité fonctionnelle associée à une tumeur carcinoïde.
E34.1 Autres conditions d'hypersécrétion d'hormones intestinales
E34.2 Sécrétion hormonale ectopique, non classée ailleurs
E34.3 Petite taille [nanisme], non classée ailleurs.
Petite taille:
. SAI
. constitutionnel
. Type Laron
. psychosocial
Exclus : progéria (E34.8)
Syndrome de Russell-Silver (Q87.1)
membres raccourcis avec déficit immunitaire (D82.2)
petite taille:
. achondroplasique (Q77.4)
. hypochondroplasique (Q77.4)
. pour des syndromes dysmorphiques spécifiques
(coder ces syndromes ; voir Index)
. nutritionnel (E45)
. hypophyse (E23.0)
. rénal (N25,0)
E34.4 Grandeur constitutionnelle.
E34.5 Syndrome de résistance aux androgènes. Pseudohermaphrodisme masculin avec résistance aux androgènes.
Violation de la réception hormonale périphérique. Syndrome de Reifenstein. Féminisation testiculaire (syndrome)
E34.8 Autres troubles endocriniens précisés. Dysfonctionnement de la glande pinéale. Progéria
E34.9 Trouble endocrinien, sans précision.
Violation:
. endocrinien SAI
. hormonale SAI
E35 Troubles des glandes endocrines lors de maladies classées ailleurs
E35.0 Troubles de la glande thyroïde dans les maladies classées ailleurs.
Tuberculose thyroïdienne (A18.8)
E35.1 Troubles surrénaliens dans les maladies classées ailleurs.
Maladie d'Addison d'étiologie tuberculeuse (A18.7). Syndrome de Waterhouse-Friderichsen (méningocoque) (A39.1)
E35.8 Troubles d'autres glandes endocrines dans des maladies classées ailleurs
DYSFONCTIONNEMENT NUTRITIONNEL (E40-E46)
Note. Le degré de malnutrition est généralement évalué à l’aide de mesures de poids corporel exprimées en écarts types par rapport à la moyenne d’une population de référence. Pas de prise de poids chez les enfants ni signe de perte de poids
Un changement de poids chez les enfants ou les adultes ayant déjà effectué une ou plusieurs mesures de poids est généralement un indicateur de malnutrition. Si une seule mesure du poids corporel est disponible, le diagnostic repose sur des hypothèses et n'est considéré comme définitif que si d'autres tests cliniques et de laboratoire sont effectués. Dans des cas exceptionnels, lorsqu'il n'existe aucune information sur le poids corporel, les données cliniques sont prises comme base. Si le poids corporel d'un individu est inférieur à la moyenne de la population de référence, une malnutrition sévère est hautement probable lorsque la valeur observée est inférieure de 3 écarts types ou plus à la moyenne de la population de référence ; malnutrition modérée si la valeur observée est de 2 ou plus mais moins de 3 écarts-types en dessous de la moyenne, et malnutrition légère si la valeur de poids observée est de 1 ou plus mais moins de 2 écarts-types en dessous de la moyenne du groupe de référence.
A l'exclusion de : malabsorption intestinale (K90.-)
anémie nutritionnelle (D50-D53)
conséquences de la malnutrition protéino-énergétique (E64.0)
maladie débilitante (B22.2)
jeûne (T73.0)
E40 Kwashiorkor
Malnutrition sévère, accompagnée d'œdèmes nutritionnels et de troubles de la pigmentation de la peau et des cheveux
E41 Folie nutritionnelle
Malnutrition sévère accompagnée de marasme
Exclus : kwashiorkor sénile (E42)
E42 Kwashiorkor sénile
Malnutrition protéino-énergétique sévère [comme dans E43] :
. forme intermédiaire
. avec des symptômes de kwashiorkor et de marasme
E43 Malnutrition protéino-énergétique sévère, sans précision
Perte de poids sévère chez les enfants ou les adultes, ou incapacité à prendre du poids chez un enfant, entraînant un poids observé au moins 3 écarts types inférieur à la moyenne du groupe de référence (ou une perte de poids similaire mesurée par d'autres méthodes statistiques) . Si une seule mesure du poids est disponible, une émaciation grave est susceptible de se produire lorsque le poids mesuré est inférieur de 3 écarts types ou plus à la moyenne de la population de référence. La faim gonfle
E44 Malnutrition protéino-énergétique modérée et légère
E44.0 Carence protéino-énergétique modérée. Perte de poids chez les enfants ou les adultes ou incapacité à prendre du poids chez un enfant entraînant un poids corporel estimé inférieur à la moyenne
pour la population de référence de 2 écarts-types ou plus mais moins de 3 écarts-types (ou
réduction similaire du poids corporel reflétée par d’autres méthodes statistiques). Si une seule mesure du poids corporel est disponible, une malnutrition protéino-énergétique modérée est très probable lorsque le poids corporel détecté est inférieur de 2 écarts types ou plus à la moyenne de la population de référence.
E44.1 Légère malnutrition protéino-énergétique. Perte de poids chez les enfants ou les adultes ou incapacité à prendre du poids chez un enfant entraînant un poids corporel estimé inférieur à la moyenne
pour la population de référence d’au moins 1 mais de moins de 2 écarts-types (ou une réduction similaire du poids corporel mesurée par d’autres méthodes statistiques). Si une seule mesure du poids corporel est disponible, une malnutrition protéino-énergétique légère est très probable lorsque le poids corporel détecté est inférieur de 1 ou plus mais de moins de 2 écarts types à la moyenne de la population de référence.
E45 Retard de développement dû à une malnutrition protéino-énergétique
Nutritionnel :
. petite taille (nanisme)
. retard de croissance
Retard de développement physique dû à la malnutrition
E46 Malnutrition protéino-énergétique, sans précision
Malnutrition SAI
Déséquilibre protéine-énergie SAI
AUTRES TYPES DE MALNUTRITION (E50-E64)
Exclus : anémie nutritionnelle (D50-D53)
Carence en vitamine A E50
A l'exclusion de : conséquences d'une carence en vitamine A (E64.1)
E50.0 Carence en vitamine A avec xérose conjonctivale
E50.1 Carence en vitamine A avec plaques de Bitot et xérose conjonctivale. Plaque de Bito chez un jeune enfant
E50.2 Carence en vitamine A avec xérose cornéenne
E50.3 Carence en vitamine A avec ulcération cornéenne et xérose
E50.4 Carence en vitamine A avec kératomalacie
E50.5 Carence en vitamine A avec cécité nocturne
E50.6 Carence en vitamine A avec cicatrices cornéennes xérophtalmiques
E50.7 Autres manifestations oculaires d'une carence en vitamine A Xérophtalmie SAI.
E50.8 Autres manifestations d'une carence en vitamine A.
Kératose folliculaire) due à une insuffisance
Xeoderma) vitamine A (L86)
E50.9 Carence en vitamine A, sans précision. Hypovitaminose A SAI
E51 Carence en thiamine
A l'exclusion de : conséquences d'une carence en thiamine (E64.8)
E51.1 Prends-le, prends-le.
Prends-le:
. forme sèche
. forme humide (I98.8)
E51.2 Encéphalopathie de Wernicke
E51.8 Autres manifestations d'une carence en thiamine
E51.9 Carence en thiamine, sans précision
E52 Carence en acide nicotinique [pellagre]
Échec:
. niacine (-tryptophane)
. nicotinamide
Pellagre (alcoolique)
À l'exclusion de : conséquences d'une carence en niacine (E64.8)
E53 Carence en autres vitamines B
A l'exclusion de : conséquences d'une carence en vitamine B (E64.8)
anémie par carence en vitamine B12 (D51.-)
E53.0 Carence en riboflavine. Ariboflavinose
E53.1 Carence en pyridoxine. Carence en vitamine B6.
À l'exclusion de : anémie sidéroblastique sensible à la pyridoxine (D64.3)
E53.8 Insuffisance d'autres vitamines B spécifiées.
Échec:
. biotine
. cyanocobalamine
. folate
. acide folique
. acide pantothénique
. vitamine B12
E53.9 Carence en vitamine B, sans précision
E54 Carence en acide ascorbique
Carence en vitamine C. Scorbut.
A l'exclusion de : anémie due au scorbut (D53.2)
conséquences d'une carence en vitamine C (E64.2)
E55 Carence en vitamine D
ostéoporose (M80-M81)
conséquences du rachitisme (E64.3)
E55.0 Le rachitisme est actif.
Ostéomalacie :
. pour enfants
. jeune
Exclus : rachitisme :
. intestinal (K90.0)
. Couronne (K50.-)
. inactif (E64.3)
. rénal (N25,0)
. résistant à la vitamine D (E83.3)
E55.9 Carence en vitamine D, sans précision. Carence en vitamine D
E56 Carence en autres vitamines
À l'exclusion de : conséquences d'autres carences en vitamines (E64.8)
E56.0 Carence en vitamine E
E56.1 Carence en vitamine K.
À l'exclusion de : déficit en facteur de coagulation dû à un déficit en vitamine K (D68.4)
Carence en vitamine K chez le nouveau-né (P53)
E56.8 Carence en autres vitamines
E56.9 Carence en vitamines, sans précision
E58 Carence nutritionnelle en calcium
À l'exclusion de : troubles du métabolisme du calcium (E83.5)
conséquences d'une carence en calcium (E64.8)
E59 Carence nutritionnelle en sélénium
Maladie de Keshan
A l'exclusion de : conséquences d'une carence en sélénium (E64.8)
E60 Carence nutritionnelle en zinc
E61 Autres piles insuffisantes
S'il est nécessaire d'identifier le médicament à l'origine de la carence, utiliser un code de cause externe supplémentaire (classe XX).
A l'exclusion de : troubles du métabolisme minéral (E83.-)
dysfonctionnement thyroïdien associé à une carence en iode (E00-E02)
E61.0 Carence en cuivre
E61.1 Carence en fer.
A l'exclusion de : anémie ferriprive (D50.-)
E61.2 Carence en magnésium
E61.3 Carence en manganèse
E61.4 Carence en chrome
E61.5 Carence en molybdène
E61.6 Carence en vanadium
E61.7 Insuffisance de nombreux nutriments
E61.8 Insuffisance d’autres nutriments spécifiés
E61.9 Carence nutritionnelle non précisée
E63 Autres types de malnutrition
Exclus : déshydratation (E86)
troubles de la croissance (R62.8)
problèmes pour nourrir un nouveau-né (P92. -)
conséquences de la malnutrition et autres carences nutritionnelles (E64.-)
E63.0 Carence en acides gras essentiels
E63.1 Apport déséquilibré en éléments nutritionnels
E63.8 Autres types spécifiés de malnutrition
E63.9 Malnutrition, sans précision. Cardiomyopathie par malnutrition SAI+ (I43.2)
E64 Conséquences de la malnutrition et autres carences nutritionnelles
E64.0 Conséquences d'un déficit protéino-énergétique.
À l'exclusion de : retard de développement dû à une malnutrition protéino-énergétique (E45)
E64.1 Conséquences d'une carence en vitamine A
E64.2 Conséquences d'une carence en vitamine C
E64.3 Conséquences du rachitisme
E64.8 Conséquences d'autres carences en vitamines
E64.9 Conséquences de carences nutritionnelles non précisées
OBÉSITÉ ET AUTRES TYPES DE SURNUTRITION (E65-E68)
E65 Dépôt graisseux localisé
Coussinets adipeux
E66 Obésité
À l'exclusion de : dystrophie adiposogénitale (E23.6)
lipomatose :
. SAI (E88.2)
. douloureux [maladie de Dercum] (E88.2)
Syndrome de Prader-Willi (Q87.1)
E66.0 Obésité due à un apport énergétique excessif
E66.1 Obésité médicamenteuse.
S'il est nécessaire d'identifier le médicament, utilisez un code supplémentaire pour les causes externes (classe XX).
E66.2 Obésité extrême accompagnée d'hypoventilation alvéolaire. Syndrome de Pickwickien
E66.8 Autres formes d'obésité. Obésité morbide
E66.9 Obésité, sans précision. Obésité simple SAI
E67 Autres types de redondance de puissance
À l'exclusion de : excès alimentaires SAI (R63.2)
conséquences d'une alimentation excessive (E68)
E67.0 Hypervitaminose A
E67.1 Hypercaroténémie
E67.2 Syndrome de mégadose de vitamine B6
E67.3 Hypervitaminose D
E67.8 Autres formes spécifiées d’excès nutritionnel
E68 Conséquences d'une alimentation redondante
TROUBLES DU MÉTABOLISME (E70-E90)
À l'exclusion de : syndrome de résistance aux androgènes (E34.5)
hyperplasie surrénalienne congénitale (E25.0)
Syndrome d'Ehlers-Danlos (Q79.6)
anémie hémolytique causée par des troubles enzymatiques (D55. -)
Syndrome de Marfan (Q87.4)
Déficit en 5-alpha réductase (E29.1)
E70 Troubles du métabolisme des acides aminés aromatiques
E70.0 Phénylcétonurie classique
E70.1 Autres types d'hyperphénylalaninémie
E70.2 Troubles du métabolisme de la tyrosine. Alcaptonurie. Hypertyrosinémie. Ochronose. Tyrosinémie. Tyrosinose
E70.3 Albinisme.
Albinisme:
. oculaire
. cutanéo-oculaire
Syndrome:
. Chediak(-Steinbrink)-Higashi
. Croix
. Hermanski-Pudlak
E70.8 Autres troubles du métabolisme des acides aminés aromatiques.
Infractions :
. échange d'histidine
. métabolisme du tryptophane
E70.9 Troubles du métabolisme des acides aminés aromatiques, sans précision
E71 Troubles du métabolisme des acides aminés à chaîne ramifiée et des acides gras
E71.0 Maladie du sirop d'érable
E71.1 Autres types de troubles du métabolisme des acides aminés à chaîne ramifiée. Hyperleucine-isoleucinémie. Hypervalinémie.
Acidémie isovalérique. Acidémie méthylmalonique. Acidémie propionique
E71.2 Troubles du métabolisme des acides aminés à chaîne ramifiée, sans précision
E71.3 Troubles du métabolisme des acides gras. Adrénoleucodystrophie [Addison-Schilder].
Déficit musculaire en carnitine palmityl transférase.
À l'exclusion de : Maladie de Refsum (G60.1)
Maladie de Schilder (G37.0)
Syndrome de Zellweger (Q87.8)
E72 Autres troubles du métabolisme des acides aminés
Exclus : écarts par rapport à la norme sans manifestations de maladie (R70-R89)
infractions :
. métabolisme des acides aminés aromatiques (E70. -)
. métabolisme des acides aminés à chaîne ramifiée (E71.0-E71.2)
. métabolisme des acides gras (E71.3)
. échange de purines et de pyrimidines (E79.-)
goutte (M10.-)
E72.0 Troubles du transport des acides aminés. Cystinose. Cystinurie.
Syndrome de Fanconi (-de Toni) (-Maladie de Hartnap). Le syndrome de Lowe.
A l'exclusion de : troubles du métabolisme du tryptophane (E70.8)
E72.1 Troubles du métabolisme des acides aminés soufrés. Cystathioninurie.
Homocystinurie. Méthioninémie. Déficit en sulfite oxydase.
À l'exclusion de : déficit en transcobalamine II (D51.2)
E72.2 Troubles du métabolisme du cycle de l'urée. Argininémie. Argininosuccinaacidurie. Citrullinémie. Hyperammoniémie.
A l'exclusion de : troubles du métabolisme de l'ornithine (E72.4)
E72.3 Troubles du métabolisme de la lysine et de l'hydroxylysine. Acidurie glutarique. Hydroxylysinémie. Hyperlysinémie
E72.4 Troubles du métabolisme de l'ornithine. Ornithinémie (types I, II)
E72.5 Troubles du métabolisme de la glycine. Hyperhydroxyprolinémie. Hyperprolinémie (types I, II). Hyperglycinémie non cétonique.
Sarcosinémie
E72.8 Autres troubles spécifiés du métabolisme des acides aminés.
Infractions :
. métabolisme des acides aminés bêta
. cycle gamma-glutamyle
E72.9 Troubles du métabolisme des acides aminés, sans précision
E73 Intolérance au lactose
E73.0 Déficit congénital en lactase
E73.1 Déficit secondaire en lactase
E73.8 Autres types d'intolérance au lactose
E73.9 Intolérance au lactose, sans précision
E74 Autres troubles du métabolisme des glucides
À l'exclusion de : augmentation de la sécrétion de glucagon (E16.3)
diabète sucré (E10-E14)
hypoglycémie SAI (E16.2)
mucopolysaccharidose (E76.0-E76.3)
E74.0 Maladies du stockage du glycogène. Glycogénose cardiaque.
Maladie:
. Andersen
. Corey
. Forbes
. Gersa
. McArdle
. Pompe
. Taureau
. Gierke
Déficit en phosphorylase hépatique
E74.1 Troubles du métabolisme du fructose. Fructosurie essentielle.
Déficit en fructose-1,6-biphosphatase. Intolérance héréditaire au fructose
E74.2 Troubles du métabolisme du galactose. Déficit en galactokinase. Galactosémie
E74.3 Autres troubles de l'absorption des glucides dans l'intestin. Absorption altérée du glucose-galactose.
Carence en saccharose.
A l'exclusion de : intolérance au lactose (E73.-)
E74.4 Troubles du métabolisme du pyruvate et de la glyconéogenèse.
Échec:
. phosphoénolpyruvate carboxykinase
. pyruvate :
. carboxylase
. déshydrogénases
Exclus : avec anémie (D55.-)
E74.8 Autres troubles spécifiés du métabolisme des glucides. Pentosurie essentielle. Oxalose. Oxalurie.
Glycosurie rénale
E74.9 Trouble du métabolisme des glucides, sans précision
E75 Troubles du métabolisme des sphingolipides et autres maladies du stockage des lipides
Exclus : mucolipidose, types I-III (E77.0-E77.1)
Maladie de Refsum (G60.1)
E75.0 Gangliosidose-GM2.
Maladie:
. Sandhoff
. Tay Sachs
Gangliosidose GM2 :
. SAI
. adultes
. juvénile
E75.1 Autres gangliosidoses.
Gangliosidose :
. SAI
. GM1
. GM3
Mucolipidose IV
E75.2 Autres sphingolipidoses.
Maladie:
. Fabry(-Anderson)
. Gaucher
. Krabbé
. Nieman-Pick
Le syndrome de Faber. Leucodystrophie métachromatique. Déficit en sulfatase.
À l'exclusion de : adrénoleucodystrophie (Addison-Schilder) (E71.3)
E75.3 Sphingolipidose, sans précision
E75.4 Lipofuscinose des neurones.
Maladie:
. Latte
. Bilshovsky-Janski
. Koufsa
. Spielmeier-Vogt
E75.5 Autres troubles du stockage des lipides. Cholestérose cérébrotendineuse [Van Bogart-Scherer-Epstein]. La maladie de Wolman
E75.6 Maladie du stockage lipidique, sans précision
E76 Troubles du métabolisme des glycosaminoglycanes
E76.0 Mucopolysaccharidose, type I.
Syndrome :
. Gurler
. Gurler-Scheie
. Scheie
E76.1 Mucopolysaccharidose, type II. syndrome de Günther
E76.2 Autres mucopolysaccharidoses. Déficit en bêta-glucuronidase. Mucopolysaccharidoses types III, IV, VI, VII
Syndrome:
. Maroto-Lami (léger) (lourd)
. Morquio (-like) (classique)
. Sanfilippo (type B) (type C) (type D)
E76.3 Mucopolysaccharidose, sans précision
E76.8 Autres troubles du métabolisme des glycosaminoglycanes
E76.9 Trouble du métabolisme des glycosaminoglycanes, sans précision
E77 Troubles du métabolisme des glycoprotéines
E77.0 Défauts dans la modification post-traductionnelle des enzymes lysosomales. Mucolipidose II.
Mucolipidose III [pseudopolydystrophie de Hurler]
E77.1 Défauts de dégradation des glycoprotéines. Aspartylglucosaminurie. Fucosidose. Mannosidose. Sialidose [mucolipidose I]
E77.8 Autres troubles du métabolisme des glycoprotéines
E77.9 Troubles du métabolisme des glycoprotéines, sans précision
E78 Troubles du métabolisme des lipoprotéines et autres lipidémies
À l'exclusion de : sphingolipidose (E75.0-E75.3)
E78.0 Hypercholestérolémie pure. Hypercholestérolémie familiale. Hyperlipoportéinémie de Fredrickson, type Iia.
Hyper-bêta-lipoprotéinémie. Hyperlipidémie, groupe A. Hyperlipoprotéinémie à lipoprotéines de basse densité
E78.1 Hyperglycéridémie pure. Hyperglycéridémie endogène. Hyperlipoportéinémie de Fredrickson, type IV.
Hyperlipidémie, groupe B. Hyperpré-bêta-lipoprotéinémie. Hyperlipoprotéinémie avec très faible taux de lipoprotéines
densité
E78.2 Hyperlipidémie mixte. Bêta-lipoprotéinémie étendue ou flottante.
Hyperlipoportéinémie de Fredrickson, types IIb ou III. Hyperbétalipoprotéinémie avec pré-bêta lipoprotéinémie.
Hypercholestérolémie avec hyperglycéridémie endogène. Hyperlipidémie, groupe C. Xanthome tuboéruptif.
Xanthome tubéreux.
À l'exclusion de : cholestérose cérébrotendineuse [Van Bogaert-Scherer-Epstein] (E75.5)
E78.3 Hyperchylomicronémie. Hyperlipoportaïnémie de Fredrickson, types I ou V.
Hyperlipidémie, groupe D. Hyperglycéridémie mixte
E78.4 Autres hyperlipidémies. Hyperlipidémie combinée familiale
E78.5 Hyperlipidémie, sans précision
E78.6 Carence en lipoprotéines. Lipoprotéinémie bêta-bêta. Carence en lipoprotéines de haute densité.
Hypo-alpha lipoprotéinémie. Hypo-bêta-lipoprotéinémie (familiale). Déficit en lécithine cholestérol acyltransférase. Maladie de Tanger
E78.8 Autres troubles du métabolisme des lipoprotéines
E78.9 Troubles du métabolisme des lipoprotéines, sans précision
E79 Troubles du métabolisme des purines et des pyrimidines
Exclut : calculs rénaux (N20,0)
déficits immunitaires combinés (D81.-)
goutte (M10.-)
Anémie orotacidurique (D53.0)
xeroderma pigmentosum (Q82.1)
E79.0 Hyperuricémie sans signes d'arthrite inflammatoire et de ganglions goutteux. Hyperuricémie asymptomatique
E79.1 Syndrome de Lesch-Nychen
E79.8 Autres troubles du métabolisme des purines et des pyrimidines. Xanthinurie héréditaire
E79.9 Perturbation du métabolisme des purines et des pyrimidines, sans précision
E80 Troubles du métabolisme de la porphyrine et de la bilirubine
Comprend : défauts de la catalase et de la peroxydase
E80.0 Porphyrie érythropoïétique héréditaire. Porphyrie érythropoïétique congénitale.
Protoporphyrie érythropoïétique
E80.1 Porphyrie cutanée lente
E80.2 Autres porphyries. Coproporphyrie héréditaire
Porphyrie :
. SAI
. aigu intermittent (hépatique)
S'il est nécessaire d'identifier la cause, utilisez un code de cause externe supplémentaire (classe XX).
E80.3 Défauts de catalase et de peroxydase. Acatalasie [Takahara]
E80.4 Le syndrome de Gilbert
E80.5 Syndrome de Crigler-Najjar
E80.6 Autres troubles du métabolisme de la bilirubine. Syndrome de Dubin-Johnson. Syndrome des rotors
E80.7 Trouble du métabolisme de la bilirubine, sans précision
E83 Troubles du métabolisme minéral
À l'exclusion de : carence nutritionnelle en minéraux (E58-E61)
troubles parathyroïdiens (E20-E21)
Carence en vitamine D (E55.-)
E83.0 Troubles du métabolisme du cuivre. Maladie de Menkès [maladie des cheveux bouclés] [cheveux d'acier]. La maladie de Wilson
E83.1 Troubles du métabolisme du fer. Hémochromatose.
Exclus : anémie :
. carence en fer (D50.-)
. sidéroblastique (D64.0-D64.3)
E83.2 Troubles du métabolisme du zinc. Acrodermatite entéropathique
E83.3 Troubles du métabolisme du phosphore. Déficit en phosphatase acide. Hypophosphatémie familiale. Hypophosphatasie.
Résistant à la vitamine D :
. ostéomalacie
. rachitisme
A l'exclusion de : ostéomalacie de l'adulte (M83.-)
ostéoporose (M80-M81)
E83.4 Troubles du métabolisme du magnésium. Hypermagnésémie. Hypomagnésémie
E83.5 Troubles du métabolisme du calcium. Hypercalcémie hypocalciurique familiale. Hypercalciurie idiopathique.
Exclut : chondrocalcinose (M11.1-M11.2)
hyperparathyroïdie (E21.0-E21.3)
E83.8 Autres troubles du métabolisme minéral
E83.9 Trouble du métabolisme minéral, sans précision
E84 Mucoviscidose
Inclus : mucoviscidose
E84.0 Mucoviscidose avec manifestations pulmonaires
E84.1 Mucoviscidose avec manifestations intestinales. Iléus méconial (P75)
E84.8 Mucoviscidose avec d'autres manifestations. Mucoviscidose avec manifestations combinées
E84.9 Fibrose kystique, sans précision
E85 Amylose
A l'exclusion de : Maladie d'Alzheimer (G30.-)
E85.0 Amylose familiale héréditaire sans neuropathie. Fièvre méditerranéenne familiale.
Néphropathie amyloïde héréditaire
E85.1 Amylose familiale héréditaire neuropathique. Polyneuropathie amyloïde (portugais)
E85.2 Amylose familiale héréditaire, sans précision
E85.3 Amylose systémique secondaire. Amylose associée à l'hémodialyse
E85.4 Amylose limitée. Amylose localisée
E85.8 Autres formes d'amylose
E85.9 Amylose, sans précision
E86 Réduction du volume de liquide
Déshydratation. Diminution du volume de plasma ou de liquide extracellulaire. Hypovolémie
À l'exclusion de : déshydratation néonatale (P74.1)
choc hypovolémique:
. NSA (R57.1)
. postopératoire (T81.1)
. traumatique (T79.4)
E87 Autres troubles du métabolisme eau-sel ou de l'équilibre acido-basique
E87.0 Hyperosmolarité et hypernatrémie. Excès de sodium. Surcharge de sodium
E87.1 Hypoosmolarité et hyponatrémie. Carence en sodium.
À l'exclusion de : syndrome d'altération de la sécrétion d'hormone antidiurétique (E22.2)
E87.2 Acidose.
Acidose:
. SAI
. lactique
. métabolique
. respiratoire
Exclut : acidose diabétique (E10-E14 avec quatrième chiffre commun.1)
E87.3 Alcalose.
Alcalose :
. SAI
. métabolique
. respiratoire
E87.4 Déséquilibre mixte acido-basique
E87.5 Hyperkaliémie. Excès de potassium [K]. Surcharge de potassium [K]
E87.6 Hypokaliémie. Carence en potassium [K]
E87.7 Hypervolémie.
A l'exclusion de : œdème (R60.-)
E87.8 Autres troubles de l'équilibre eau-sel, non classés ailleurs.
Déséquilibre électrolytique SAI. Hyperchlorémie. Hypochlorémie
E88 Autres troubles métaboliques
À l'exclusion de : histiocidose X (chronique) (D76.0)
S'il est nécessaire d'identifier le médicament à l'origine du trouble métabolique, utilisez un code de cause externe supplémentaire (classe XX).
E88.0 Troubles du métabolisme des protéines plasmatiques, non classés ailleurs. Déficit en alpha-1 antitrypsine.
Bis-albuminémie.
A l'exclusion de : troubles du métabolisme lipoprotéique (E78.-)
gammapathie monoclonale (D47.2)
hyper-gammaglobulinémie polyclonale (D89.0)
Macroglobulinémie de Waldenström (C88.0)
E88.1 Lipodystrophie, non classée ailleurs. Lipodystrophie SAI.
Exclut : Maladie de Whipple (K90.8)
E88.2 Lipomatose, non classée ailleurs.
Lipomatose :
. SAI
. douloureux [maladie de Dercum]
E88.8 Autres troubles métaboliques spécifiés. Adénolipomatose Lonois-Bansod. Triméthylaminurie
E88.9 Trouble métabolique, sans précision
E89 Troubles endocriniens et métaboliques consécutifs à des actes médicaux, non classés ailleurs
E89.0 Hypothyroïdie résultant d'interventions médicales.
Hypothyroïdie radio-induite. Hypothyroïdie postopératoire
E89.1 Hypoinsulinémie survenant après des procédures médicales. Hyperglycémie après ablation du pancréas.
Hypoinsulinémie postopératoire
E89.2 Hypoparathyroïdie résultant d'interventions médicales. Tétanie parathyroïdienne
E89.3 Hypopitutarisme survenant après des interventions médicales. Hypopituitarisme radio-induit
E89.4 Dysfonctionnement ovarien résultant d'interventions médicales
E89.5 Hypofonction testiculaire après une intervention médicale
E89.6 Hypofonction du cortex surrénalien (médulla) qui survient après une intervention médicale
E89.8 Autres troubles endocriniens et métaboliques survenant après des procédures médicales
E89.9 Trouble endocrinien et métabolique consécutif à une intervention médicale, sans précision
12171 0
Goitre toxique diffus (DTZ)- Maladie de Basedow, maladie de Parry, maladie de Basedow - une maladie auto-immune génétiquement déterminée qui se manifeste par une hyperproduction persistante d'hormones thyroïdiennes par une glande thyroïde hypertrophiée de manière diffuse sous l'influence d'auto-anticorps spécifiques stimulant la thyroïde.
CODE CIM-10
E05.0. Thyrotoxicose avec goitre diffus.
Épidémiologie
L'incidence est d'environ 5 à 6 cas pour 100 000 habitants. La maladie se manifeste le plus souvent entre 16 et 40 ans, majoritairement chez les femmes.Étiologie et pathogenèse
Le rôle principal dans le développement de la maladie appartient à la prédisposition héréditaire avec l'inclusion de mécanismes auto-immuns. 15 % des patients atteints de DTD ont des proches atteints de la même maladie. Environ 50 % des proches des patients possèdent des auto-anticorps thyroïdiens circulants. Les facteurs provoquants peuvent être un traumatisme mental, des maladies infectieuses, une grossesse, la prise de fortes doses d'iode et une exposition prolongée au soleil. Les lymphocytes B et les plasmocytes reconnaissent par erreur les récepteurs thyroïdiens de la TSH comme des antigènes et produisent des auto-anticorps stimulant la thyroïde. En se liant aux récepteurs TSH des thyrocytes comme la TSH, ils déclenchent la réaction adénylate cyclase et stimulent la fonction thyroïdienne. En conséquence, sa masse et sa vascularisation augmentent, ainsi que la production d'hormones thyroïdiennes.Image clinique
La thyréotoxicose avec thyréotoxicose est généralement sévère. Un excès d'hormones thyroïdiennes a un effet toxique sur tous les organes et systèmes, active les processus cataboliques, à la suite desquels les patients perdent du poids, apparaissent une faiblesse musculaire, une fièvre légère, une tachycardie et une fibrillation auriculaire. Une dystrophie myocardique, une insuffisance surrénale et insulinique et une cachexie se développent ensuite.En règle générale, la glande thyroïde est uniformément élargie, de consistance souple et élastique, indolore et se déplace lors de la déglutition.
Le tableau clinique est dû à l'influence d'un excès d'hormones thyroïdiennes sur les organes et systèmes du corps. La complexité et la multiplicité des facteurs impliqués dans la pathogenèse déterminent la variété des manifestations cliniques de la maladie.
Lors de l'analyse des plaintes et des résultats d'un examen objectif, divers symptômes sont identifiés qui peuvent être combinés en plusieurs syndromes.
Dommages au système nerveux central et périphérique. Sous l'influence d'un excès d'hormones thyroïdiennes, les patients présentent une excitabilité accrue, une labilité psycho-émotionnelle, une diminution de la concentration, des larmoiements, de la fatigue, des troubles du sommeil, des tremblements des doigts et de tout le corps (syndrome du poteau télégraphique), une transpiration accrue, un dermographisme rouge persistant et une augmentation réflexes tendineux.
Syndrome oculaire causée par une hypertonie des muscles du globe oculaire et de la paupière supérieure due à une perturbation de l'innervation autonome sous l'influence d'un excès d'hormones thyroïdiennes.
- Le signe de Dalrymple(exophtalmie, exophtalmie thyroïdienne) - élargissement de la fissure palpébrale avec apparition d'une bande blanche de sclère entre l'iris et la paupière supérieure.
- Le symptôme de Graefe- décalage de la paupière supérieure par rapport à l'iris lors de la fixation du regard sur un objet se déplaçant lentement vers le bas. Dans ce cas, une bande blanche de sclère reste entre la paupière supérieure et l'iris.
- Le signe de Kocher- lorsque vous fixez votre regard sur un objet qui se déplace lentement vers le haut, une bande blanche de sclère subsiste entre la paupière inférieure et l'iris.
- Le signe de Stellwag- de rares clignements des paupières.
- Signe de Möbius- perte de capacité à fixer le regard de près. En raison de la faiblesse des muscles adducteurs des yeux, les globes oculaires fixés sur un objet proche divergent et reprennent leur position d'origine.
- Symptôme de Repnev-Melekhov- "regard en colère".
Ophtalmopathie endocrinienne se manifeste cliniquement par des troubles des muscles extraoculaires, des troubles trophiques et une exophtalmie. Les patients sont gênés par des douleurs, une vision double, une sensation de « sable » dans les yeux et des larmoiements. Les conjonctivites et les kératites se développent souvent avec une ulcération de la cornée due à son dessèchement lorsque les paupières ne se ferment pas complètement. Parfois, la maladie prend une évolution maligne, une asymétrie et une saillie des globes oculaires se développent jusqu'à ce que l'un d'eux tombe complètement hors de l'orbite.
Il existe 3 stades de l'ophtalmopathie endocrinienne :
I - gonflement des paupières, sensation de « sable » dans les yeux, larmoiement ;
II - diplopie, abduction limitée des globes oculaires, parésie du regard vers le haut ;
III - fermeture incomplète de la fissure palpébrale, ulcération cornéenne, diplopie persistante, atrophie du nerf optique.
Les dommages au système cardiovasculaire se manifestent par une tachycardie, une fibrillation auriculaire, le développement d'une dystrophie myocardique dishormonale (« cœur thyrotoxique ») et une pression pulsée élevée. Les troubles cardiaques sont associés à la fois à l'effet toxique direct des hormones sur le myocarde et à une augmentation du travail du cœur en raison des besoins accrus des tissus périphériques en oxygène dans des conditions de métabolisme accru. En raison d’une augmentation de l’accident vasculaire cérébral et du débit cardiaque et d’une accélération du flux sanguin, la pression artérielle systolique (TA) augmente. Un souffle systolique apparaît au sommet du cœur et sur les artères carotides. Une diminution de la pression artérielle diastolique dans la thyréotoxicose est associée au développement d'une insuffisance surrénalienne et à une diminution de la production de glucocorticoïdes, principaux régulateurs du tonus de la paroi vasculaire.
Dommages au système digestif se manifeste par des selles instables avec tendance à la diarrhée, des crises de douleurs abdominales et parfois une jaunisse, associée à une insuffisance hépatique.
Dommages à d'autres glandes :
Un dysfonctionnement du cortex surrénalien, en plus de réduire la pression artérielle diastolique, provoque également une hyperpigmentation de la peau. Une pigmentation apparaît souvent autour des yeux - le signe de Jellinek.
La dégradation accrue du glycogène et l'entrée de grandes quantités de glucose dans le sang obligent le pancréas à fonctionner en mode de tension maximale, ce qui conduit finalement à son insuffisance - un diabète sucré thyroïdien se développe. L'évolution du diabète sucré existant chez les patients atteints de DTG s'aggrave considérablement.
D'autres troubles hormonaux chez les femmes comprennent le dysfonctionnement ovarien avec irrégularités menstruelles et la mastopathie fibrokystique (mastopathie thyréotoxique, maladie de Velyaminov) et chez les hommes - la gynécomastie.
Syndrome de trouble catabolique se manifeste par une perte de poids accompagnée d'une augmentation de l'appétit, d'une légère fièvre et d'une faiblesse musculaire.
Myxœdème prétibial- une autre manifestation du DTZ - se développe dans 1 à 4 % des cas. Dans ce cas, la peau de la face antérieure de la jambe devient enflée et épaissie. Des démangeaisons et un érythème surviennent souvent.
Diagnostique
En règle générale, le diagnostic DTZ ne pose pas de difficultés. Un tableau clinique caractéristique, une augmentation du taux de T 3, T 4 et des anticorps spécifiques, ainsi qu'une diminution significative du taux de TSH dans le sang permettent de poser un diagnostic. L'échographie et la scintigraphie permettent de distinguer la thyréotoxicose des autres maladies manifestées par la thyréotoxicose. L'échographie révèle une hypertrophie diffuse de la glande thyroïde, le tissu est hypoéchogène, la cartographie Doppler révèle une vascularisation accrue - une image d'un « feu thyroïdien ». Lors de l'analyse des radionucléides, une absorption accrue d'iode radioactif par l'ensemble de la glande thyroïde est observée.Traitement
Objectifs du traitement
Élimination de la thyréotoxicose et des troubles associés. Actuellement, trois méthodes de traitement du DTG sont utilisées : les médicaments, la chirurgie et le traitement à l'iode radioactif.Traitement médical
Un traitement médicamenteux est indiqué en cas de DTG nouvellement diagnostiqué. Pour bloquer la synthèse des hormones thyroïdiennes, des thyréostatiques sont utilisés : thiamazole, propylthiouracile. Le thiamazole est prescrit à une dose allant jusqu'à 30 à 60 mg/jour, le propylthiouracile jusqu'à 100 à 400 mg/jour. Après avoir atteint un état euthyroïdien, la dose du médicament est réduite à une dose d'entretien (5 à 10 mg/jour) et pour prévenir l'effet goitrogène du thyréostatique, de la lévothyroxine sodique (25 à 50 mcg/jour) est en outre prescrite. La combinaison d'un agent thyrostatique avec de la lévothyroxine sodique fonctionne selon le principe « bloquer et remplacer ». Le traitement symptomatique comprend la prescription de sédatifs et de β-bloquants (propranolol, aténolol). En cas d'insuffisance surrénalienne ou d'ophtalmopathie endocrinienne, des glucocorticoïdes (prednisolone 5-30 mg/jour) doivent être prescrits. Le traitement se poursuit pendant 1 à 1,5 ans sous le contrôle des niveaux de TSH. Une rémission persistante pendant plusieurs années après l'arrêt des thyréostatiques indique une guérison. Avec un petit volume de glande thyroïde, la probabilité d'un effet positif d'un traitement conservateur est de 50 à 70 %.Chirurgie
Le traitement chirurgical est indiqué en l'absence d'effet durable du traitement conservateur ; grand volume de la glande thyroïde (plus de 35 à 40 ml), lorsqu'il est difficile d'attendre un effet d'un traitement conservateur ; thyréotoxicose compliquée et syndrome de compression.La préparation à la chirurgie repose sur les mêmes principes que dans le traitement des patients atteints de thyréotoxicose. En cas d'intolérance aux thyréostatiques, de fortes doses d'iode sont utilisées, qui ont un effet thyréostatique. Pour ce faire, une courte préparation est réalisée avec la solution de Lugol. Au cours de 5 jours, la dose du médicament est augmentée de 1,5 à 3,5 cuillères à café par jour avec l'apport obligatoire de 100 mcg/jour de lévothyroxine sodique. En cas de thyréotoxicose sévère, la préparation préopératoire comprend des glucocorticoïdes et une plasmaphérèse.
La résection sous-fasciale sous-totale de la glande thyroïde est réalisée selon O.V. Nikolaev, laissant au total 4 à 7 g de parenchyme thyroïdien des deux côtés de la trachée. On pense que le maintien de cette quantité de tissu fournit au corps de manière adéquate des hormones thyroïdiennes. Ces dernières années, on a tendance à pratiquer une thyroïdectomie pour DTG, ce qui élimine le risque de rechute de thyréotoxicose, mais conduit à une hypothyroïdie sévère, comme dans le traitement à l'iode radioactif.
Le pronostic après la chirurgie est généralement bon. L'hypothyroïdie postopératoire ne doit guère être considérée comme une complication. Il s'agit plutôt d'un résultat naturel de l'opération, associé à un radicalisme excessif, justifié par la prévention des rechutes de thyréotoxicose. Dans ces cas, un traitement hormonal substitutif est nécessaire. La rechute de la thyréotoxicose survient dans 0,5 à 3 % des cas. Si la thérapie thyréostatique n'a aucun effet, un traitement à l'iode radioactif ou une réintervention est prescrit.
Complications postopératoires
La complication la plus grave après une intervention chirurgicale pour un goitre toxique est la crise thyréotoxique. La mortalité en période de crise est très élevée, atteignant 50 % ou plus. Actuellement, cette complication est extrêmement rarement observée.Le rôle principal dans le mécanisme de développement de la crise est attribué à l'insuffisance surrénalienne aiguë et à l'augmentation rapide du niveau de fractions libres de T 3 et T 4 dans le sang. Dans le même temps, les patients sont agités, la température corporelle atteint 40 ° C, la peau devient humide, chaude et hyperémique, une tachycardie sévère et une fibrillation auriculaire surviennent. Par la suite, une défaillance cardiovasculaire et multiviscérale se développe rapidement, ce qui devient la cause du décès.
Le traitement est effectué dans une unité de soins intensifs spécialisée. Il comprend l'administration de fortes doses de glucocorticoïdes, de thyréostatiques, de solution de Lugol, de β-bloquants, de désintoxication et de sédation, de correction des troubles hydriques et électrolytiques et de l'insuffisance cardiovasculaire.
Pour prévenir une crise thyréotoxique, l'intervention chirurgicale n'est réalisée qu'après compensation de la thyréotoxicose.
Traitement à l'iode radioactif
Le traitement à l'iode radioactif (131 I) repose sur la capacité des rayons β à provoquer la mort de l'épithélium folliculaire de la glande thyroïde, suivi de son remplacement par du tissu conjonctif. Ce processus s'accompagne d'une suppression de l'activité fonctionnelle de l'organe et d'un soulagement de la thyréotoxicose. Actuellement, la thérapie à l'iode radioactif est reconnue comme le moyen le plus rationnel de traiter le goitre toxique diffus en l'absence d'indications directes de chirurgie (présence d'un syndrome de compression). Un tel traitement est particulièrement indiqué en cas de risque chirurgical élevé (maladies concomitantes graves, vieillesse), lorsque le patient refuse catégoriquement l'intervention chirurgicale et lorsque la maladie rechute après un traitement chirurgical.SUIS. Shulutko, V.I. Semikov






